| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学试题《物质的量》高频试题巩固(2019年最新版)(二)
参考答案:B 本题解析:两种气体的物质的量不相等,则分子数不相等,选项A不正确;但二者的原子都是2amol,所以选项B正确;选项C不正确,前者含有2amol电子,后者含有4mol电子;选项D不正确,前者是2ag,后者是8ag,答案选B。 本题难度:一般 2、选择题 对于同质量的SO2和SO3,下列说法正确的是 |
参考答案:
本题解析:
本题难度:一般
3、填空题 FeO、Fe2O3、Fe3O4三种纯的氧化物中,与等量铁原子相结合的氧原子的质量比为?,与等量氧原子相结合的铁原子的物质的量之比为? ?。
参考答案:6∶9∶8 12∶8∶9?
本题解析:等量铁原子时,假定铁原子的物质的量均为1 mol,则氧原子的物质的量分别为1 mol、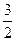 mol、
mol、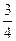 mol,其质量之比即物质的量之比,为:?
mol,其质量之比即物质的量之比,为:?
1 mol∶mol∶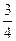 mol=6∶9∶8
mol=6∶9∶8
等量氧原子时,假定氧原子的物质的量均为1 mol,则铁原子的物质的量分别为1 mol、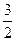 mol、
mol、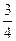 mol,其物质的量之比为:1 mol∶
mol,其物质的量之比为:1 mol∶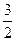 mol∶
mol∶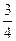 mol=12∶8∶9。
mol=12∶8∶9。
本题难度:简单
4、选择题 等质量的Fe2O3和MgO粉末分别完全溶解于相同体积的稀硫酸中,得到的Fe2(SO4)3和MgSO4溶液的浓度分别为a mol/L和b mol/L,则a 和b的关系正确的是
A.a ="=" b
B.2a ="=" b
C.4a ="=" b
D.a ="=" 4 b
参考答案:C
本题解析:设质量为mg,Fe2O3和MgO的物质的量分别为m/160 mol、m/40 mol,两种物质都溶解,根据质量守恒定律,a: b=" (m/160):(" m/40)=1:4,即4a ="=" b。故选C。
点评:本题考查学生利用离子反应方程式的计算,明确金属离子与氢氧根离子的关系,盐中金属离子与硫酸根离子的关系是解答本题的关键,难度不大。
本题难度:简单
5、选择题 下列溶液中,与100 ml 0.5 mol/L NaCl溶液所含的Cl-的物质的量浓度相同的是
A.100ml 0.5mol/L MgCl2溶液
B.200ml 0.25mol/L HCl溶液
C.50ml 1mol/L NaCl溶液
D.200ml 0.25mol/L CaCl2溶液
参考答案:D
本题解析:氯离子浓度与溶液体积多少无关,0.5 mol/L NaCl溶液所含的Cl-的物质的量浓度为0.5 mol/L;0.5mol/L MgCl2溶液Cl-的物质的量浓度为1 mol/L;0.25mol/L HCl溶液Cl-的物质的量浓度0.25mol/L;1mol/L? NaCl溶液Cl-的物质的量浓度1mol/L;0.25mol/L CaCl2溶液Cl-的物质的量浓度0.5mol/L;
本题难度:简单
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高中化学知识点总结《硫酸》答题.. | |