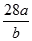1��ѡ���� ��NA��ʾ�����ӵ�������ֵ������������ȷ���ǣ�?��
A�������£�42.0g��ϩ�ͱ�ϩ�Ļ�������к��е�̼ԭ����Ϊ3NA
B��100 mL 18.4 mol��L-1����������ͭ��Ӧ������S02�ķ�����Ϊ0.92 NA
C��1 L 0.1 mol��L-1�Ĵ�����Һ�����������Ӻͷ�������Ϊ0��1 NA
D��1.2g NaHS04�����������Ӻ������ӵ�����Ϊ0.03 NA
�ο��𰸣�A
�����������ϩ�ͱ�ϩ�����ʽ��ͬ������CH2��42.0g������к���3mol̼ԭ�ӣ�����A��ȷ��Ũ�����ڷ�Ӧ�����У�Ũ�Ȼ���ϡ����ϡ������ͭ�Dz���Ӧ�ģ�����B��Ӧ��С��0.92 NA��B����ȷ��C����ȷ����Ϊ���д�����ˮ���ӡ�NaHS04�����������Ӻ������ӵĸ���֮����1�U1�ģ�D����ȷ����ѡA��
�����Ѷȣ�һ��
2�������� þ�����������仯�������������������й㷺��Ӧ�á�
��1��þ���Ͻ����ڷɻ�����ҵ������3��90��þ���Ͻ�����������2mol/Lϡ����������0��2mol���������㲢ȷ��þ���Ͻ������ʵ���n(Mg): n(Al)=?��
��2�����������Ҫ�ɷ�ΪFeS2(��������ֻ��SiO2)�����������ԭ�ϡ�ȡij������10g�������Ŀ��������գ�4FeS2+11O2��2Fe2O3+8SO2������ַ�Ӧ����ȴ���Ƶù�������Ϊ7��4g������SiO2����Ӧ��������������FeS2����������Ϊ?��
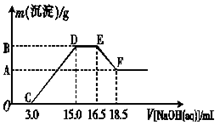
��3������һ���������ۺ�������ɵĻ�����100 mLϡ�����ַ�Ӧ����Ӧ���������κ�����ų�������Ӧ��ij�����Һ������4��00 mol��L��1��NaOH��Һ������NaOH��Һ���������������������Ĺ�ϵ��ͼ��ʾ(��Ҫʱ�ɼ��ȣ�����������ˮ�е��ܽ�)����������A�����ֵ��?��
��4���������������������������֡�ȡij������ĩ28��12g(����ֻ��Fe��C)�����������г�ַ�Ӧ���õ�CO2����224mL(��״����)��
�ټ���˸�����ĩ������̼�����ʵ���֮��Ϊ?����������ȣ���
����ȡ���ݲ�ͬ����������������ĩ�ֱ�ӵ�100mL��ͬŨ�ȵ�ϡH2SO4�У���ַ�Ӧ��õ�ʵ���������±���ʾ��
ʵ�����
| ��
| ��
| ��
|
���������ĩ��������g��
| 2��812
| 5��624
| 8��436
|
��������������L������״����
| 1��120
| 2��240
| 2��800
|
?
���������Һ�����ʵ���Ũ��Ϊ?��
����������ʵ����м�������m�˸�����ĩ�����㷴Ӧ������ʣ��Ĺ�������Ϊ?g (����3λС��)
�ο��𰸣���1��1:2 ��2�֣�?
��2��78%��2�֣�?
��3��0��856��2�֣�
��4����50��1?
��1��25 mol/L
�� (m��5��624)��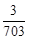 g��
g��
���������
��1���⣺��Mg��Al�����ʵ���Ϊx��y
Mg+H2SO4 ="Mg" SO4+ H2��? 2 Al+3H2SO4 = Al2 (SO4)3+ 3H2��
x? x? 2? 3
y? 3/2 y
x+ 3/2 y =0��2? 24 x+ 27*y=3��90? x=0��05? y=0��1
��þ���Ͻ������ʵ���n(Mg): n(Al)= 0��05: 0��1=1:2
��2���⣺��FeS2������Ϊx
4FeS2? +11O2=2Fe2O3 +8SO2?�Sm
4*120?��4*120-2*160��
x? (10-7��4)
x=7��8?
����������FeS2����������Ϊ7��8*100%/10=78%
��3����HN O3�����ʵ���Ũ��Ϊx��Al�����ʵ���Ϊy��Fe�����ʵ���Ϊz
OC��HN O3����--NaOH? EF��Al-----Al��OH��3����----- NaOH����------Na AlO2
100x? 4*3? y? 4*��18��5-16��5��/1000
x=0��12? y=0��008?
CD��? Al����3 OH������Al��OH��3? Fe���� 3 OH������Fe��OH��3
3? 1? 3? 1
0��024? 0��008? 4*��15-3��/1000-0��024?0��008
A����������������������� 107*0��008=0��856��g��
��4����nCO2= 0��224/22��4=0��01(mol)
C���� CO2
0��01? 0��01?nFe=(28��12-0��01*12)/56=0��5(mol)
�˸�����ĩ������̼�����ʵ���֮��Ϊ?nFe:nC=0��5:? 0��01=50��1?
���ɱ���֪����������������������������������n H2=2��8/22��4=0��125(mol)
H2SO4------ H2
0��05
��������Һ�����ʵ���Ũ��ΪC=n/V=0��125/0��1=1��25�� mol/L��
�ۣ���ǡ���ܽ�ʱ����������Ϊx������ʵ��I��III��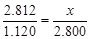 ?x��7��030g
?x��7��030g
��ʱ����ĸ���������Ϊm��7��030��5��624��1��406g
�ٵ�������ĩ�е���δȫ���ܽ�ʱ����m��1��406g
��Ӧ������ʣ����������Ϊm��5��624��0��125��56����m��1��376��g
�ڵ�������ĩ�е���ȫ���ܽ�ʱ����m��1��406g
��Ӧ������ʣ����������Ϊ? (m��5��624)��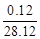 g?�� (m��5��624)��
g?�� (m��5��624)��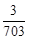 g��
g��
�����Ѷȣ�����
3��ѡ���� ��֪a��N2���� b�����ӣ����ӵ���������ֵΪ��
A��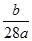
B��
C��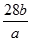
D��