1、选择题 下列有关分子晶体的说法中正确的是( )
A.分子内均存在共价键
B.分子间一定存在范德华力
C.分子间一定存在氢键
D.其结构一定为分子密堆积
参考答案:B
本题解析:稀有气体元素组成的晶体中,不存在由多个原子组成的分子,而是原子间通过范德华力结合成晶体,所以不存在任何化学键,故A项错误。分子间作用力包括范德华力和氢键,范德华力存在于所有的分子晶体中,而氢键只存在于含有与电负性较强的N、O、F原子结合的氢原子的分子之间或者分子内,所以B项正确,C项错误。只有只存在范德华力的分子晶体才采取分子密堆积的方式,所以D选项也是错误的。
本题难度:简单
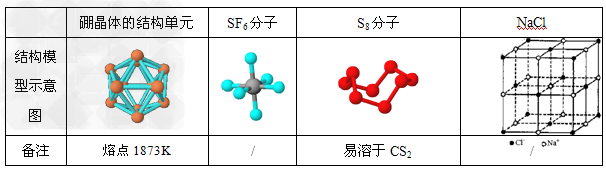
2、选择题 观察下列模型并结合有关信息,判断有关说法正确的是
[? ]
A.单质硼属分子晶体,其结构单元B12中含有30个B-B键,含20个正三角形
B.SF6是由极性键构成的非极性分子
C.固态硫S8属于原子晶体?
D.NaCl熔化和溶于水均能产生自由移动的离子,且破坏的是同种作用力
参考答案:BD
本题解析:
本题难度:一般
3、填空题 下图为一个金属铜的晶胞,请完成以下各题。

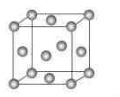
1)该晶胞“实际”拥有的铜原子数是?个。
2)该晶胞称为?。
A.六方晶胞? B.体心立方晶胞? C.面心立方晶胞
3)此晶胞立方体的边长为a cm,Cu的相对原子质量为64。阿伏加德罗常数为NA 。金属铜的晶体密度ρ为?g/cm3。(用a、NA?表示)。
4)铜原子采取的这种堆积方式的空间利用率为?。(填数值)
参考答案:(4分)
1) 4。2)C。3)256/(a3×NA)。4)74%。
本题解析:1)顶点的被8个晶胞共用,面心的被2个晶胞共用,故该晶胞“实际”拥有的铜原子数是8*(1/8)+6*(1/2)=4个。
2)该晶胞面心中有金属铜,故选C。
3)D原子半径为r,令晶胞的棱长为x,则2x2=(4r)2,所以x= 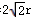 r,所以晶胞的体积V=
r,所以晶胞的体积V= 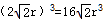 .晶胞中含有的铜原子数目为8×(1/8) +6×(1/2)=4,所以晶胞的质量为4×Mr/ NAg,所以晶体的密度为
.晶胞中含有的铜原子数目为8×(1/8) +6×(1/2)=4,所以晶胞的质量为4×Mr/ NAg,所以晶体的密度为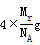 =256/(a3×NA)。
=256/(a3×NA)。
4)晶体铜晶胞是面心立方晶胞,故铜原子采取的这种堆积方式的空间利用率为74%。
点评:本题考查的是晶胞的计算的相关知识,题目难度中,考查学生分析问题、解决问题及计算的能力。
本题难度:一般
4、选择题 氮化碳是化工行业已合成的一种硬度比金刚石还大的晶体,已知在此化合物中各元素均处于其最高或最低价态,下列有关“氮化碳”的叙述正确的是?(?)
A.氮化碳的化学式为C4N3
B.氮化碳的晶体类型为离子晶体
C.构成氮化碳晶体的微粒是碳原子和氮原子,且构成空间网状结构
D.氮化碳晶体中存在的微粒间的作用力有共价键和分子间作用力
参考答案:C
本题解析:氮化碳是化工行业已合成的一种硬度比金刚石还大的晶体,说明应该是原子晶体,所以BD不正确,C正确。氮元素的最低价是-3价,碳元素是+4价,所以其化学式为C3N4。答案选C。
本题难度:一般
5、选择题 金属的下列性质中与金属晶体结构无关的是(?)
A.导电性
B.化学反应中易失去电子
C.延展性
D.硬度
参考答案:B
本题解析:金属晶体中原子间以金属键相互结合。A、金属晶体中存在许多自由电子,在外加电场的作用下定向移动形成电流,正确;B、在化学反应中金属易失电子与金属原子的结构有关,与晶体结构无关,错误;C、金属在受外力时金属的各原子层发生相对滑动,但不改变原来的排列方式,所以具有很好的延展性,正确;D、硬度的大小与金属键的强弱有关,正确,答案选B。
本题难度:简单