1、实验题 (15分)在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应。?应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”。请回答该实验中的问题。
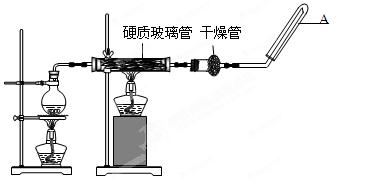
(1)写出该反应的反应方程式? ?;
?; 并指明该氧化还原反应的还原剂是?,氧化剂是?。
并指明该氧化还原反应的还原剂是?,氧化剂是?。
(2)圆底烧瓶中盛装的水,该装置受热后的主要作用是??;烧瓶底部放置了几片碎瓷片,其作用是? ?。
(3)试管中收集气体是?,如果要在A处玻璃管处点燃该气体,则必须对该气体进行?。
参考答案:.(15分)
(1)? 3Fe+ 4H2O(气)= 高温= Fe3O4+ 4 H23分,以下空各2分?Fe???H2O

本题解析:略
本题难度:一般
2、填空题 还原铁粉是粉末冶金工业的重要原料,利用生产钛 白的副产品绿矾制备还原铁粉的工业流程如下:
白的副产品绿矾制备还原铁粉的工业流程如下:
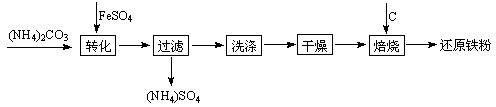
⑴干燥过程主要是为了脱去游离水和结晶水,过程中会有少量FeCO3・nH2O被空气氧化为FeOOH,其化学方程式为?。
⑵取干燥后的FeCO3样品12.49 g焙烧至600℃,质量变为8.00 g,继续加热最终得到Fe 6.16 g,则600℃产物的可能组成为?,计算FeCO3样品中FeCO3与FeOOH的质量。
⑶若将28.12 g还原铁粉(含少量FexC)在氧气流中加热,得到标准状况下的CO2 224 mL;将相同质量的还原铁粉与足量硫酸反应,得到标准状况下的H2 10.752 L,计算FexC的化学式。(假设还原铁粉仅含两种物质)
参考答案:
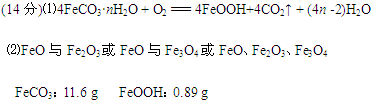
(3)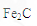
本题解析:略
本题难度:一般
3、实验题 铁不能与冷、热水反应,但是能与水蒸气反应。实验装置如图所示。在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下铁与水蒸气反应的实验。请回答:
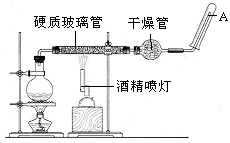
(1)写出该反应的化学方程式?。
(2)实验前必须对整套装置进行的操作是________,实验开始时应先点燃?(填“酒精灯”或“酒精喷灯”),实验结束时应先熄灭?(填“酒精灯”或“酒精喷灯”)。
(3)圆底烧瓶中盛有水,该装置受热后的主要作用是?;烧瓶里应事先放置?,其作用是?;干燥管中盛装的物质是________。
(4)待硬质玻璃管冷却后,取少许其中的固体物质溶于稀硫酸得溶液B,取少量溶液B滴加?溶液,若?(填实验现象),则说明溶液B中含有Fe3+。
参考答案:(1)3Fe+4H2O(g) Fe3O4+4H2;(2)检查装置的气密性,酒精灯,酒精喷灯;
Fe3O4+4H2;(2)检查装置的气密性,酒精灯,酒精喷灯;
(3)为实验提供水蒸气,碎瓷片,防止暴沸,碱石灰(合理答案也给分);(4)KSCN,溶液变红色(其他合理答案也给分)。
本题解析:(1)高温下,铁与水蒸气反应生成四氧化三铁和氢气,化学方程式为3Fe+4H2O(g) Fe3O4+4H2;(2)实验前必须对整套装置进行的操作是检查装置的气密性,实验开始时,要先排尽装置中的空气,应先点燃酒精灯,实验结束时,应是产物在水蒸气中冷却,应先熄灭酒精喷灯; (3)圆底烧瓶中盛有水,该装置受热后的主要作用是为实验提供水蒸气;烧瓶里应事先放置碎瓷片,其作用是防暴沸;干燥管中盛装的物质是碱石灰。(4)考查Fe3+的检验;待硬质玻璃管冷却后,取少许其中的固体物质溶于稀硫酸得溶液B,取少量溶液B滴加KSCN溶液,若溶液变红色,则说明溶液B中含有Fe3+。
Fe3O4+4H2;(2)实验前必须对整套装置进行的操作是检查装置的气密性,实验开始时,要先排尽装置中的空气,应先点燃酒精灯,实验结束时,应是产物在水蒸气中冷却,应先熄灭酒精喷灯; (3)圆底烧瓶中盛有水,该装置受热后的主要作用是为实验提供水蒸气;烧瓶里应事先放置碎瓷片,其作用是防暴沸;干燥管中盛装的物质是碱石灰。(4)考查Fe3+的检验;待硬质玻璃管冷却后,取少许其中的固体物质溶于稀硫酸得溶液B,取少量溶液B滴加KSCN溶液,若溶液变红色,则说明溶液B中含有Fe3+。
本题难度:简单
4、填空题 【化学一选修2:化学与技术】(15分)
利用硫酸工业废渣(主要含Fe2O3、SiO2、Al2O3、MgO等杂质)制备氧化铁的工艺流程如下:
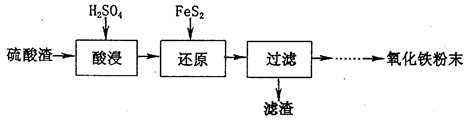
(1)“酸浸”中硫酸要适当过量,目的是:①提高铁的浸出率,②__________________。
(2)“还原”是将Fe3+转化为Fe2+,同时FeS2被氧化为SO ,该反应的离子方程式为____________.
,该反应的离子方程式为____________.
(3)为测定“酸浸”步骤后溶液中Fe3+的量以控制加入FeS2的量。
实验步骤为:准确量取一定体积的酸浸后的溶液于锥形瓶中,加入HCl、稍过量SnCl2,再加HgCl2除去过量的SnCl2,以二苯胺磺酸钠为指示剂,用K2Cr2O7标准溶液滴定,有关反应方程式如下:
2Fe3++Sn2++6Cl-===2Fe2++SnCl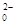
Sn2++4Cl-+2HgCl2="==" SnCl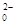 +Hg2Cl2↓
+Hg2Cl2↓
6Fe2++ Cr2O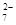 +14H+===6Fe3++2Cr3++7H2O
+14H+===6Fe3++2Cr3++7H2O
①若SnCl2不足量,则测定的Fe3+量__________(填“偏高”、“偏低”、“不变”,下同)。
②若不加HgCl2,则测定的Fe3+量偏高,其原因是_____________。
(4)①可选用______________(填试剂)检验滤液中含有Fe3+。产生Fe3+的原因是_________________(用离子反应方程式表示)。
②已知部分阳离子以氢氧化物形式沉淀时溶液的,pH见下表:
沉淀物
| Fe(OH)3
| Fe(OH)2
| Al(OH)3
| Mg(OH)2
| Mn(OH)2
|
开始沉淀
| 2.3
| 7.5
| 3.4
| 9.4
| 8.3
|
完全沉淀
| 3.2
| 9.7
| 4.4
| 12.4
| 9.8
|
实验可选用的试剂有:稀HNO3、Ba(NO3)2溶液、酸性KMnO4溶液、NaOH溶液,要求制备过程中不产生有毒气体。请完成由“过滤”后的溶液模拟制备氧化铁的实验步骤:
a.氧化:________________________________;b.沉淀:_____________________________;
c.分离,洗涤;d.烘干,研磨。
参考答案:(1)抑制Fe3+的水解(2分)
(2)14Fe3++FeS2+8H2O ===15Fe2++2SO +16H+(2分)
+16H+(2分)
(3)①偏低,②若不加HgCl2,溶液中含有Sn2+,也可以被酸性高锰酸钾氧化,消耗的酸性高锰酸钾氧化偏大,则测定的Fe3+量偏高。(2分)
(4)①KSCN(2分);4Fe2++O2+4H+ ===4Fe3++H2O (2分);
②a.向溶液中加入过量的酸性高锰酸钾溶液,搅拌(2分);
b.滴加NaOH溶液,调节溶液的pH为3.2~3.8(2分)
本题解析:(1) 酸浸”中硫酸要适当过量,抑制Fe3+的水解;
(2)由信息Fe3+转化为Fe2+,同时FeS2被氧化为SO ,在利用氧化还原反应配平方程式:14Fe3++FeS2+8H2O ===15Fe2++2SO
,在利用氧化还原反应配平方程式:14Fe3++FeS2+8H2O ===15Fe2++2SO +16H+;
+16H+;
(3)①若SnCl2不足量,Fe3+没有完全还原为Fe2+,则测定的Fe3+量偏低,②若不加HgCl2,溶液中含有Sn2+,也可以被酸性高锰酸钾氧化,消耗的酸性高锰酸钾氧化偏大,则测定的Fe3+量偏高。
(4)①检验滤液中含有Fe3+是KSCN溶液;Fe2+的氧化反应是:4Fe2++O2+4H+ ===4Fe3++H2O;
②a.向溶液中加入过量的酸性高锰酸钾溶液,搅拌;b.滴加NaOH溶液,调节溶液的pH为3.2~3.8,使Fe3++完全沉淀。
本题难度:困难
5、填空题 金属单质A与盐酸反应生成浅绿色溶液B,同时放出气体C。如果在B溶液中通入氯气,则B转变成棕黄色溶液D,将溶液D分为两份,一份加入几滴KSCN溶液,溶液变成血红色,另一份加入A,则棕黄色溶液D重新变成浅绿色溶液B。则:
(1)各物质的化学式分别是:A________ ,B________ ,C________ ,D________;
(2)有关反应的离子方程式有:
① B→D___________________________;
② D→B____________________________。
参考答案:(1)Fe? FeCl2? H2? FeCl3
(2)①2Fe2++Cl2=2Fe3++Cl―
②2Fe3++Fe=3Fe2+
本题解析:氯化亚铁溶液呈浅绿色,氯化铁溶液呈棕黄色,前者可被氯气氧化为后者,氯化铁遇KSCN溶液变红,氯化铁溶液被铁还原为氯化亚铁,铁与盐酸反应生成氯化亚铁和氢气,由此推断A、B、C、D分别为Fe、FeCl2、H2、FeCl3;根据离子方程式和氧化还原反应方程式的配平可知,B→D的反应式为2Fe2++Cl2=2Fe3++Cl―;D→B的反应式为2Fe3++Fe=3Fe2+。
本题难度:简单