1、选择题 2010年上海世博会中国馆(东方之冠)给人强烈的视觉冲击,它的主体结构是用国产Q460钢制成的。下列有关说法正确的是(?)
A.冶炼钢铁常采用热分解法
B.Q460是含铁、碳、硅、锰、硫、磷等元素的合金钢,其中铁和锰不属于主族元素
C.铝热法炼铁的反应需要高温的条件,所以是吸热反应
D.增加炼铁高炉的高度可以减少尾气CO的排放
参考答案:B
本题解析:冶炼钢铁常采用热还原法,A项错误。铁属于第Ⅷ族,锰属于第ⅦB族,B项正确。铝热反应属于放热反应,C项错误。增加炼铁高炉的高度并不能减少CO的排放,D项错误。
本题难度:一般
2、计算题 在某硫酸铜溶液中,加入一个质量为1.12g的铁片,经过一段时间,铁片表面覆盖了一层红色的铜,取出洗净、烘干,称重,质量变为1.16g。计算在这个化学反应中溶解了铁多少克?
参考答案:0.28g
本题解析:Fe+CuSO4=FeSO4+Cu,从化学方程可以看出,铁片质量的增加,与铁的溶解和铜的析出直接联系,每溶解56g铁,将析出64g铜,会使铁片质量增加:64g-56g=8g
根据铁片增加的质量(1.16g-1.12g),可计算出溶解的Fe的质量和析出的Cu的质量。
解:设溶解的Fe为xg,析出的Cu为yg
Fe+CuSO4=Cu+FeSO4?△m
56?64?64-56
x?y?1.16-1.12
则: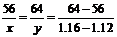 ,解得:x=0.28g? y=0.32g
,解得:x=0.28g? y=0.32g
答:在这个化学反应中溶解了铁0.28g。
本题难度:一般
3、选择题 将1.12g铁粉加入25mL2mol/L的FeCl3溶液中,充分反应后,其结果是(? )
A.铁恰好将Fe3+全部还原
B.往反应后溶液中滴入KSCN溶液,不显红色
C.溶液变为浅绿色
D.Fe2+和Fe3+物质的量之比为6:1
参考答案:D
本题解析:将1.12g铁粉加入到25mL 2mol?L-1的氯化铁溶液中,铁粉的物质的量n=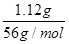 ?=0.02mol。氯化铁的物质的量n=C×V=2mol?L-1×0.025L=0.05mol,铁粉与氯化铁的离子反应方程式为:Fe+2Fe3+=3Fe2+,根据反应的物质的量之比等于计量数之比知,0.02mol铁粉完全反应需要0.04mol氯化铁。所以氯化铁剩余0.01mol,生成的Fe2+的物质的量为0.06mol。A选项错误。B选项错误,由于溶液中有三节铁离子剩余,故显红色。C选项,由于有三价铁离子剩余,故溶液应为浅绿与红棕的混合色。错误。D选项正确。
?=0.02mol。氯化铁的物质的量n=C×V=2mol?L-1×0.025L=0.05mol,铁粉与氯化铁的离子反应方程式为:Fe+2Fe3+=3Fe2+,根据反应的物质的量之比等于计量数之比知,0.02mol铁粉完全反应需要0.04mol氯化铁。所以氯化铁剩余0.01mol,生成的Fe2+的物质的量为0.06mol。A选项错误。B选项错误,由于溶液中有三节铁离子剩余,故显红色。C选项,由于有三价铁离子剩余,故溶液应为浅绿与红棕的混合色。错误。D选项正确。
本题难度:一般
4、填空题 无水硝酸铜极易吸水,加热到210℃升华,它和Cu(NO3)2 ・3H2O晶体的化学性质有较大差异, Cu(NO3)2 ・3H2O晶体加热到170℃分解。已知:乙酸乙酯的沸点为77 ℃。
(1)加热蒸干Cu(NO3)2 溶液得不到无水硝酸铜的原因是_____________。
(2)将铜片加人到N2 O 4的乙酸乙酯溶液中可制得无水硝酸铜,同时生成NO,写出反应的化学方程式_____________;从乙酸乙醋中分离出无水硝酸铜的实验操作是_____________。
(3)为探究Cu(NO3)2 ・3H2O受热分解的产物,某探究小组利用下图装置进行实验。(图中夹持和加热装置去)
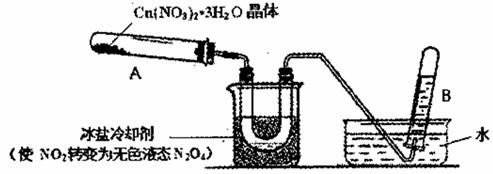
往试管A中加人研细的Cu(NO3)2 ・3H2O体并加热,观察到试管A中有红棕色气生成,最终残留黑色粉末;U型管中有液体生成,在试管B中收集到无色气体。
①当导管口不再有气池冒出时,反应停止,拆除装置的操作首先是______。
②试管B中收集到的气体一定含有______。
(4)锌与Cu(NO3)2溶液能发生反应。在一支试管中注人1 mol・L-1的Cu(NO3)2溶液,再放入一块锌片,观察到在反应初期有大量无色气泡冒出,同时锌片上析出红色固体。该小组猜想气体的成分,并设计的实验步骤,请填写下表。

参考答案:(1)Cu(NO3)2在溶液中易水解生成Cu(OH)2和易挥发的HNO3,加热,水解程度更大(2分)
(2)2N2O4+Cu=Cu(NO3)2+2NO↑(没配平扣1分,没“↑”不扣分,3分)蒸馏?(2分)
(3)①移出水槽中的导管B(其它合理答案也给分,2分)②O2(2分)(4)
设计的实验步骤
预期现象和结论
往小试管中注入空气(或使试管口露置于空气中)
若试管口气体变为红棕色,证明该气体是NO,反之不是。
将小试管的管口靠近火焰
若有爆鸣声,证明该气体是H2,反之不是
?
(上述实验两种方案,答对一种即给分,其它方案如合理也给分;结论为O2不给分,实验步骤1分,现象1分,结论2分,共4分)
本题解析:(1)Cu(NO3)2在溶液中易水解生成Cu(OH)2和易挥发的HNO3,水解吸热,加热,水解程度更大,因此加热蒸干Cu(NO3)2 溶液。
(2)将铜片加人到N2 O 4的乙酸乙酯溶液中可制得无水硝酸铜,同时生成NO,则根据原子守恒以及电荷守恒看写出该反应的化学方程式为2N2O4+Cu=Cu(NO3)2+2NO↑;由于乙酸乙酯的沸点为77 ℃,所以从乙酸乙醋中分离出无水硝酸铜的实验操作是蒸馏。
(3)①由于排水法收集气体时温度降低后容易倒吸,因此反应停止,拆除装置的操作首先是移出水槽中的导管B。
②试管A中有红棕色气生成,因此气体是NO2。最终残留黑色粉末,该黑色粉末应该是氧化铜;U型管中有液体生成,此时NO2转化为四氧化二氮。所以根据氧化还原反应中电子得失守恒可知,反应中一定还有氧化产物氧气产生,则在试管B中收集到无色气体一定含有氧气。
(4)硝酸铜溶液中铜离子水解溶液显酸性,另外NO3-还具有氧化性,因此锌与硝酸铜溶液反应生成的无色气体可能是氢气或NO。检验NO可以利用NO极易被氧化生成红棕色NO2来验证。而氢气是可燃性气体,所以可以利用爆鸣法进行验证。
本题难度:困难
5、选择题 下列各组物质不能按所示关系实现转化的是表示反应一步完成( )
A.

B.
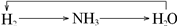
C.
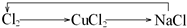
D.

参考答案:D
本题解析:
本题难度:一般