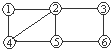
1、推断题 下图是A~O 的转化关系。已知A是一种金属单质,B、C、D、E、F、H、I、J、K常温常压下均为气体,且B、C、D、E是单质,I是一种红棕色气体,G是一种淡黄色固体,M是混合物,含有气体,J与K相遇会产生大量白烟。请回答下列问题
(1)写出G与水反应的化学方程式______________________________;写出气体E与N溶液反应的离子方程式__________________________。
(2)化合物G中含有的化学键为___________________。
(3)写出F的电子式________________,化合物O的电子式__________________。
(4)E与F反应生成气体的化学方程式为_________________________________。
参考答案:(1)2Na2O2+2H2O==4NaOH+O2↑;Cl2+2OH-==Cl-+ClO-+H2O
(2)离子键、共价键
(3)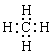 ;
;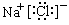
(4)CH4+Cl2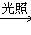 CH3Cl+HCl
CH3Cl+HCl
本题解析:
本题难度:困难
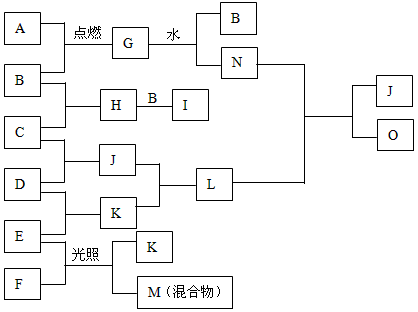
2、填空题 (6分)下图是一些常见的单质、化合物之间的转化关系图,有些反应中的部分物质被略去。反应①常被应用于野外焊接钢轨,F是海水中含有盐的主要成分,J为D、G反应产物形成的水溶液。
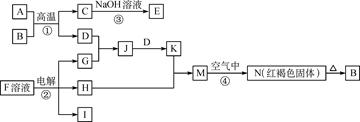
请回答下列问题:
(1)B的化学式为____________。
(2)H的电子式为____________。
(3)写出反应③的离子方程式 。
(4)写出反应④的化学方程式 。
参考答案:(6分)
(1) Fe2O3(1分) (2) 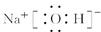 (1分)
(1分)
(3) Al2O3+2OH-===2AlO2-+H2O(2分)
(4) 4Fe(OH)2+O2+2H2O===4Fe(OH)3(2分)
本题解析:由N为红褐色固体可以确定N为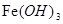 ,进而可以确定M为Fe(OH)2,
,进而可以确定M为Fe(OH)2,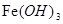 加热失水变为Fe2O3,B为Fe2O3,①常被应用于野外焊接钢轨可以得出该反应是铝热反应B为Fe2O3所以A为Al,结合C和D的性质可以确定C为Al2O3,D为Fe, F是海水中含有盐的主要成分所以F为NaCl,电解饱和食盐水的产物是Cl2,NaOH,H2,G与Fe可以发生反应所以G为Cl2,则J为Fe Cl3,K为Fe Cl2,所以H为NaOH。
加热失水变为Fe2O3,B为Fe2O3,①常被应用于野外焊接钢轨可以得出该反应是铝热反应B为Fe2O3所以A为Al,结合C和D的性质可以确定C为Al2O3,D为Fe, F是海水中含有盐的主要成分所以F为NaCl,电解饱和食盐水的产物是Cl2,NaOH,H2,G与Fe可以发生反应所以G为Cl2,则J为Fe Cl3,K为Fe Cl2,所以H为NaOH。
(1)?B的化学式Fe2O3
(2)?NaOH的电子式为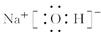
(3)?三氧化二铝与氢氧化钠反应的离子反应方程式为Al2O3+2OH-===2AlO2-+H2O
(4)?氢氧化亚铁在空气中发生变化的化学方程式是4Fe(OH)2+O2+2H2O===4Fe(OH)3
本题难度:一般
3、简答题 下方图中A~K均为中学化学中常见的物质,其中A和F是金属单质,D是最常见的溶剂.I为黄绿色气体,C的焰色反应呈黄色,K是红褐色固体.
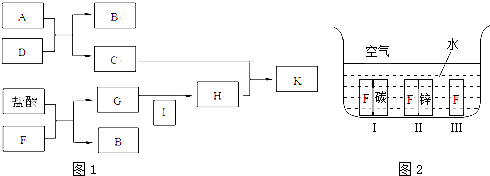
(1)A元素在周期表中位于第______周期______族.
(2)D和I反应的离子方程式为______.G+I→H的离子方程式为______.
(3)实验室常用______和______试剂检验G中的阳离子.
(4)如上方右图所示,F处于Ⅰ、Ⅱ、Ⅲ三种不同的环境中,该金属被腐蚀的速率由快到慢的顺序是(填序号)______.
参考答案:C的焰色反应呈黄色,应含有Na元素,则A应为Na,D是最常见的溶剂,应为H2O,A和D反应生成NaOH和H2,则C为NaOH,B为H2,I为黄绿色气体,应为Cl2,K是红褐色固体,应为Fe(OH)3,则H为FeCl3,G为FeCl2,F为Fe,
(1)由以上分析可知A为Na,原子核外有3个电子层,最外层电子数为1,应位于周期表第三周期、ⅠA族,
故答案为:三;ⅠA;
(2)D为H2O,I为Cl2,二者反应生成HCl和HClO,反应的离子方程式为Cl2+H2O=H++Cl-+HClO,G为FeCl2,具有还原性,可被Cl2氧化生成FeCl3,反应的离子方程式为2Fe2++Cl2=2Fe3++2Cl-,
故答案为:Cl2+H2O=H++Cl-+HClO;?2Fe2++Cl2=2Fe3++2Cl-;
(3)G为FeCl2,含有Fe2+,加入KSCN溶液不变色,但Fe2+具有还原性,可被H2O2氧化为Fe3+,溶液变红,
故答案为:H2O2、KSCN;
(4)金属腐蚀时,原电池腐蚀比化学腐蚀快,当铁为原电池负极时,易被氧化而腐蚀,当为原电池正极时,得到保护,则该金属被腐蚀的速率由快到慢的顺序是Ⅰ>Ⅲ>Ⅱ,故答案为:Ⅰ>Ⅲ>Ⅱ.
本题解析:
本题难度:一般
4、填空题 (15分)A―J是中学化学常见的物质,它们之间的转化关系如下图所示(部分产物已略去)。已知A是一种高熔点物质,D是一种红棕色固体。
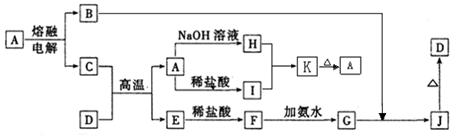
请回答下列问题:
(1)固体A的晶体类型为___________,K的化学式为?。
(2)C与D在高温下的反应在冶金工业上称为?反应,引发该反应的实验操作是_____?______。
(3)G→J的化学方程式为____________。
(4)A→H的离子方程式为?。
(5)I的水溶液pH_____7(填“>”、“<”或“=”),原因是____(用离子方程式表示)。
参考答案:(1)离子晶体 …… (2分)? Al(OH)3 ………………(2分)
(2)铝热反应………………(2分),在混合粉末上插上镁条,周围撒上少量KClO3,然后点燃镁条………………(1分)
(3)4Fe(OH)2+O2+2H2O=4Fe(OH)3………………(2分)
(4)Al2O3+2OH―=2AlO2―+H2O………………(2分)
(5)<(1分)? Al3++3H2O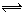 Al(OH)3+3H+………………(2分)
Al(OH)3+3H+………………(2分)
本题解析:本题属于无机框图题,关键是找准突破点。D是一种红棕色固体,所以D是氧化铁,则J是氢氧化铁。又因为A是一种高熔点物质,所以A是氧化铝,B是氧气,C是Al,E是铁,F是氯化亚铁,G是氢氧化亚铁,H是偏铝酸钠,I是氯化铝,K是氢氧化铝。氯化铝由于是强酸弱碱盐,水解显酸性,方程式为Al3++3H2O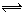 Al(OH)3+3H+。
Al(OH)3+3H+。
本题难度:一般
5、选择题 如图所示,每个编号代表下列物质中的一种物质,凡是用直线相连的两种物质均能发生化学反应.供选择的物质有:a.铁;b.稀H2SO4;c.Na2CO3溶液;d.BaCl2溶液;e.Cu(NO3)2溶液;f.MgSO4溶液.图中编号④代表的物质是( )
A.H2SO4
B.MgSO4
C.Cu(NO3)2
D.BaCl2