1、填空题 (14分)A~I分别表示中学化学中常见的一种物质,它们之间相互关系如下图所示:已知G在生产中可作为一种耐火材料,F是红褐色难溶于水的沉淀,A、B、C、D、E、F六种物质中均含同一种元素,其中I+B→A+G属于置换反应。(部分反应物、生成物没有列出)。
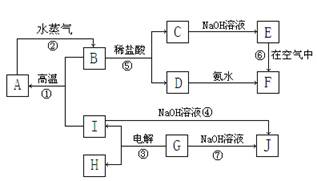
请 填写下列空白:
填写下列空白:
(1)如何检验D中阳离子:?
(2)写出反应②的化学方程式:?
写出反应⑦的离子方程式: ? ?
(3) E在空气中变成F的实验现象是?
(4)写出反应⑥的化学方程式并用单线桥标出电子转移的方向和数目:
计算该反应中若转移2 mol电子,需要标况下的O2_________________L。
参考答案:(14分)
(1)(取一定量的D溶液于试管中,滴加适量的KSCN溶液,若溶液出现血红色,则说明含Fe3+?(2分)
(2)
Al2O3 + 2OH- ="=" 2AlO2-+ H2O (每空2分)
(3)白色沉淀迅速变为灰绿色最后变为红褐色(2分)
(4)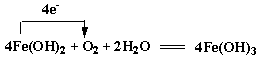 (4分)?11.2 (2分)
(4分)?11.2 (2分)
本题解析:略
本题难度:简单
2、填空题 (16分)根据提供条件推断元素,并按要求填空:
①原子核外有3个电子层,其价电子数为7,最高价氧化物化学式? ________ ,最高价氧化物对应水化物化学式? ________ ,其单质与NaOH反应的化学方程式为? ___________________________(2分)。
②短周期金属元素,最外层电子 数与电子层数相同。最高价氧化物与强酸反应的离子方程式为________________________________(2分),最高价氧化物对应水化物与氢氧化钾反应的化学方程式为? _________________________________________(2分)。
数与电子层数相同。最高价氧化物与强酸反应的离子方程式为________________________________(2分),最高价氧化物对应水化物与氢氧化钾反应的化学方程式为? _________________________________________(2分)。
③原子最外层电子数为电子层数三倍的非金属元素,与氢元素组成的化合物有两种,其电子式分别为_______、______,其单质也有两种,化学式分别为? ________、_______。(各1分)
④原子序数依次递增的四种元素,它们氢化物的质子数与电子数都与Ar相同,这些氢化物的化学式分别为? _______?、 ________?、? ________?、 ________ 。(各1分)
参考答案:(16分)(1)Cl2O7,HClO 4, HClO4 + NaOH="=Na" ClO4+H2O
4, HClO4 + NaOH="=Na" ClO4+H2O
(2)Al2O3+6H+==2Al3++3H2O? Al(OH)3+KOH==KAlO2+2H2O
(3) O2? O3? (4)HCl H2S PH3 SiH4
本题解析:略
本题难度:一般
3、推断题 A、B、C、D、E是中学常见的5种化合物,A、B是氧化物,元素X、Y的单质是生活中常见的金属,相关物质间的关系如下图所示。
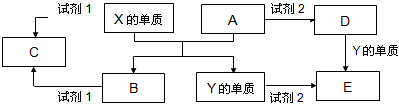
(1)X的单质与A反应的化学方程式是__________________。
(2)若试剂1是NaOH溶液,X的单质与试剂1反应的离子方程式是_______________________。
(3)若试剂1和试剂2均是稀硫酸。
①检验物质D的溶液中金属离子的方法是___________________。
②将物质C溶于水,其溶液呈酸性,原因是(用离子方程式表示)_____________________________。
③某高效净水剂是由Y(OH)SO4聚合得到的。工业上以E、稀硫酸和亚硝酸钠为原料来制备Y(OH)SO4,反应中有NO生成,该反应的化学方程式是___________________________。
参考答案:(1)Fe2O3+2Al Al2O3+2Fe
Al2O3+2Fe
(2)2Al+2H2O+2OH-==2AlO2-+3H2↑
(3)①取少量溶液于试管中,滴加几滴KSCN溶液,溶液变红色,则证明原溶液中含有Fe3+。
②Al3++3H2O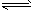 Al(OH)3+3H+;③2FeSO4+2NaNO2+H2SO4==2Fe(OH)SO4+Na2SO4+2NO↑
Al(OH)3+3H+;③2FeSO4+2NaNO2+H2SO4==2Fe(OH)SO4+Na2SO4+2NO↑
本题解析:
本题难度:困难
4、简答题 化合物A由两种常见元素组成,且A中两种元素的质量比为4:1.A有如图所示转化关系,其中B、F均为红色固体,C能使品红溶液褪色(有的反应可能在水溶液中进行,有的反应的生成物未全部给出).
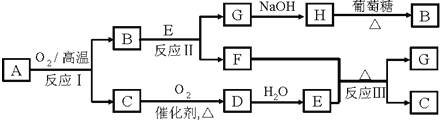
(1)写出下列物质的化学式,A______,B______,H______.
(2)反应I中还原剂与氧化剂的物质的量之比为______,
反应Ⅱ的离子方程式为______.
反应Ⅲ的化学方程式为______.
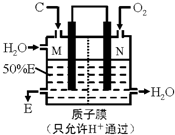
(3)某人设想用如图所示装置用电化学原理生产E,N电极是______极;写出M电极的电极反应式:______.
(4)当图中的C与O2被活性炭吸附时,也能发生放热反应生成D,为研究此反应,将C和O2放入体积为1L的恒容密闭容器中,在
500℃时发生反应,反应物浓度时间的变化如下表所示:
t(min)
浓度(mol/L) | 0 | 1 | 2 | 3 | 4 | 5 | 6
c(C)
0.054
0.034
0.018
0.012
0.008
0.006
0.006
c(O2)
0.032
0.022
0.014
0.011
0.009
0.008
0.008
|
①反应从起始至2min内的平均反应速率v(C)=______;500℃时,此反应化学平衡常数K的值为______.
②第6min时,向容器中再充入0.002molO2,同时将反应体系的温度改变为T,反应至10min时重新达到平衡,此时测得c(C)=
0.004mol/L,则温度T______(填“>”或“<”)500℃.
参考答案:(1)H和葡萄糖反应生成B为红色固体,则H为Cu(OH)2,B为Cu2O,在酸性条件下反应:Cu2O+2H+=Cu+Cu2++H2O,则E为酸,F为Cu,由C→D→E等反应可知,C为SO2,D为SO3,E为H2SO4,则G为CuSO4,A应含有Cu和S两种元素,质量比为4:1,应为Cu2S,故答案为:Cu2S;Cu2O;Cu(OH)2;
(2)反应Ⅰ为:2Cu2S+3O2?高温?.?2Cu2O+2SO2,由方程式可以看出,还原剂与氧化剂的物质的量之比为2:3,Cu2O在酸性条件下反应:Cu2O+2H+=Cu+Cu2++H2O,Cu和浓硫酸在加热条件下反应生成CuSO4和SO2,反应的化学方程式为Cu+2H2SO4(浓)?△?.?CuSO4+SO2↑+2H2O,
故答案为:2:3;Cu2O+2H+=Cu+Cu2++H2O;Cu+2H2SO4(浓)?△?.?CuSO4+SO2↑+2H2O;
(3)氧气具有氧化性,应为原电池的正极,发生还原反应,二氧化硫具有还原性,应为原电池的负极,发生氧化反应,电极反应式为SO2+2H2O-2e-=SO42-+4H+,
故答案为:正;SO2+2H2O-2e-=SO42-+4H+;
(4)①c(SO2)=0.054moL/L-0.018mol/L2min=0.018mol/(L?min),
? ?2SO2+O2

2SO3
起始:0.054mol/L 0.032mol/L
转化:0.048mol/L 0.024mol/L 0.048mol/L
平衡:0.006moL/L 0.008mol/L 0.048mol/L
k=0.04820.0062×0.008=8000,
故答案为:0.018mol/(L?min);8000;
②第6min时,向容器中再充入0.002molO2,反应至10min时重新达到平衡,此时测得c(SO2)=0.004mol/L,等效于
? 2SO2+O2

2SO3
起始:0.054mol/L 0.034mol/L? 0
转化:0.050mol/L 0.025mol/L? 0.050mol/L
平衡:0.004moL/L 0.009mol/L? 0.050mol/L
此时k=0.05020.004?2×0.009=17361>8000,说明平衡向正反应方向移动,而该反应放热,则应是降低温度,故小于500℃,
故答案为:<.
本题解析:
本题难度:一般
5、推断题 以惰性电极电解NaCl溶液或CuSO4溶液都得到三种产物A、B、C,各物质之间的转化关系如下图所示(图 中参与反应和生成的水都已略去)。已知甲是短周期元素的单质,它是日常生活中常用的包装材料。
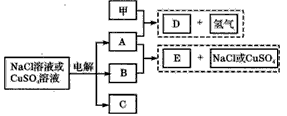
回答下列问题:
(1)甲在元素周期表中位置是____。
(2)若电解的是NaCl溶液:①A与B反应的离子方程式是___。
②若电解100mL0. 1mol・L-1NaCl溶液,阴、阳两极各产生112mL气体(标准状况),则所得溶液的pH为 ____(忽略反应前后溶液的体积变化)。
(3)若电解的是CuSO4溶液:
①E的化学式是____;电解时阳极的电极反应式是____ ;
②加热时,A的浓溶液可与B发生反应,A的浓度随时间变化的图像正确是___。
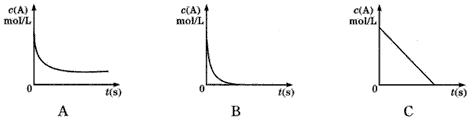
③若利用反应A+B+C→CuSO4+H2O把化学能转化为电能,所设计电池的负极材料是____(填元素符号)。
参考答案:
(1)第3周期第ⅢA族
(2)①Cl2 +2OH-==Cl-+ClO-+H2O ;②13
(3)①SO2 ;4OH--4e-==O2↑+2H2O;②A;③Cu
本题解析:
本题难度:一般