1、简答题 铜锰氧化物(CuMn2O4)能在常温下催化氧化空气中的一氧化碳和甲醛(HCHO).
(1)锰元素位于第四周期,第ⅦB族.请写出Mn2+基态的电子排布式______.NO3-的空间构型为______(用文字描述).
(2)CO和N2的结构相似,CO的结构式为______.HCHO中含有的σ键和π键数目比为______.
(3)火山喷出岩浆中含有多种硫化物.冷却时ZnS比HgS先析出,原因是______.
(4)Cu3N形成的晶体结构如图所示.与同一个N3-相连的Cu+有______个.

参考答案:(1)Mn的原子序数为25,基态原子的电子排布式为,1s22s22p63s23p63d54s2,则Mn2+基态的电子排布式可表示为1s22s22p63s23p63d5(或[Ar]3d5),NO3-中N原子形成3个δ键,没有孤电子对,则应为平面三角形,
故答案为:1s22s22p63s23p63d5;平面三角形;
(2)N2与CO为等电子体,二者结构相似,N2的结构为N≡N,则CO的结构为C≡O,
甲醛的结构式为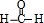 ,分子中含有2个C-H键、1个C=O键,单键为σ键,双键中具有1个σ键、1π键,故分子中σ键和π键数目比为3:1;
,分子中含有2个C-H键、1个C=O键,单键为σ键,双键中具有1个σ键、1π键,故分子中σ键和π键数目比为3:1;
故答案为:C≡O;3:1;
(3)二者均为离子晶体,ZnS晶格能大于HgS,因此ZnS先析出,故答案为:二者均为离子晶体,ZnS晶格能大于HgS,因此ZnS先析出;
(4)晶胞中黑色球数目为12×14=3,白色球数目为8×18=1,故黑色球为Cu+,白色球为N3-,由晶胞结构可知,棱上的Cu+与N3-相连,以N3-为中心,在X、Y、Z三个轴上,在每个轴上等距离的Cu+有2个,故同一个N3-相连的Cu+有6个,故答案为:6.
本题解析:
本题难度:一般
2、选择题 下列关于价电子构型3s23p4的描述正确的是
[? ]
A.该元素符号为O ?
B.该核外电子排布式为1s22s22p63s23p4 ?
C.可以与H2化合生成液态化合物 ?
D.其原子轨道式为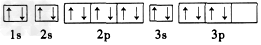
参考答案:B
本题解析:
本题难度:简单
3、填空题 [化学-选修物质结构与性质]
第一个稀有气体化合物Xe[PtF6]被合成出来后,打破了“绝对惰性”的观念.
(1)Pt与Ni在周期表中位于同一族,写出基态Ni原子核外电子排布式______.
(2)金属Pt内部原子的堆积方式与铜及干冰中CO2相同,图正方体是Pt晶胞示意图,叙述Pt原子在晶胞中位置:______.
(3)已知XeO3分子中氙原子上有1对孤对电子,则XeO3为______分子(填“极性”或“非极性”);XeO3分子中中心原子的杂化类型为______;XeO3分子实际空间构型为______
(4)一定压强,将HF和HCl混合气体降温时,首先液化的物质是______.
参考答案:(1)Ni的原子序数为28,根据能量最低原理和洪特规则可写出基态Ni原子核外电子排布式为1s22s22p63s23p63d84s2,
故答案为:1s22s22p63s23p63d84s2;
(2)铜的堆积模型为最紧密堆积,配位数为12,铜原子位于顶点和面心,与二氧化碳分子晶胞结构相似,
故答案为:正方体的八个顶点和六个面心;
(3)XeO3分子中含有3个δ键和一个孤电子对,为三角锥形分子,结构不对称,为极性分子,杂化方式为sp3杂化
故答案为:极性;sp3;三角锥形;
(4)HF含有氢键,沸点较高,易液化,故答案为:HF.
本题解析:
本题难度:一般
4、填空题 下面是s能级p能级的原子轨道图,试回答问题
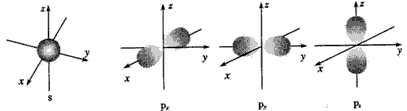
(1)s电子的原子轨道呈____形,每个s能级有________个原子轨道;p电子的原子轨道呈________形,每个p能级有____个原子轨道。
(2)s电子原子轨道、p电子原子轨道的半径与什么因素有关?是什么关系?
_________________________________
参考答案:(1)球形;1;纺锤;3
(2)与能层序数n有关;能层序数n越大,原子轨道的半径越大
本题解析:
本题难度:一般
5、填空题 以下是表示铁原子和铁离子的3种不同化学用语。
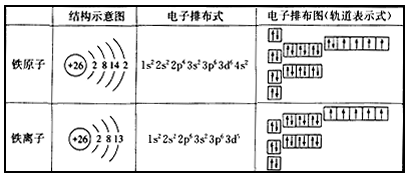
(1)铁原子最外层电子数为_______,铁在发生化学反应时,参加反应的电子可能是_____________。
(2)请你通过比较、归纳,分别说出3种不同化学用语所能反映的粒子结构信息。
______________________________
参考答案:(1)2;4s上的2个电子或4s上的2个电子和3d上的1 个电子
(2)结构示意图:能直观地反映核内的质子数和核外的电子层数及各能层上的电子数;电子排布式:能直 观地反映核外电子的能层、能级和各能级上的电子数;轨道表示式:能反映各轨道的能量的高低及各轨道上的电子分布情况,自旋方向。
本题解析:
本题难度:一般