1��ѡ���� �������и����У�����ȥ�����е����ʣ���Ӧ���е��ǣ�������
A��Cl2��HCl��----ͨ������������Һϴ��
B��FeCl2��Һ��FeCl3��----�����������ۣ�����
C��ŨHNO3��NO2��----��������ˮ
D��Na2CO3��Һ��NaHCO3��----����
�ο��𰸣�A��Cl2��HCl��������������Һ��Ӧ��Ӧ�ñ���ʳ��ˮ���ӣ���A����
B��FeCl3�������۷�Ӧ����FeCl2�������ڳ��ӣ���B��ȷ��
C��NO2��ˮ��Ӧ����NO��Ӧ�ڼ�ˮ��ͬʱͨ����������C����
D��NaHCO3�ķֽ��¶�ԼΪ150�棬������Һ��NaHCO3���ֽ⣬���Գ�ȥ����D����
��ѡB��
���������
�����Ѷȣ�һ��
2��ѡ���� �����и�������ٵ�+ɰ�ӣ���NH4Cl+NaCl������ˮ+�����NaHCO3+CaCO3������뷽����ͬ���ǣ�������
A���٢�
B���ڢ�
C���ۢ�
D���٢�
�ο��𰸣��ټ���ʱ������������+ɰ�ӿ��ü��ȷ������룻
��NH4Cl�����ֽ��������壬���ý��ȷ������룻
����ˮ�����ڱ����л��ܼ�����ˮ�����������ȡ�ķ������룻
��NaHCO3������ˮ����CaCO3�����ڣ������ܽ⡢���˵ķ������룮
���뷽����ͬ���Ǣ٢ڣ�
��ѡA��
���������
�����Ѷȣ���
3��ѡ���� Ҫ��ȥFe2O3�л��е�Al2O3����õķ�����
[? ]
A��������ϴ�ӹ���?
B��������H2��ԭ
C��������CO��ԭ?
D����NaOHϴ�ӡ�����
�ο��𰸣�D
���������
�����Ѷȣ�һ��
4������� �����̿��Ʊ�������ص���Ҫ��Ӧ���£�
��������? 3MnO2+KClO3+6KOH 3K2MnO4+KCl+3H2O
3K2MnO4+KCl+3H2O
�����绯? 3K2MnO4+2CO2=2KMnO4+MnO2��+2K2CO3
������ʵ��ܽ�ȣ�293K�����±���
?
| K2CO3
| KHCO3
| K2SO4
| KMnO4
|
�ܽ��/g
| 111
| 33.7
| 11.1
| 6.34
|
��1����ʵ���ҽ��С���������������ʱ��Ӧѡ������������ǯ��?��������ĸ��
a��������? b��������? c��������? d��������
��2������ʱ�����������ԭ����?�������������ԭ����?��
��3�����õ�ⷨҲ����ʵ��K2MnO4��ת����2K2MnO4+2H2O 2KMnO4+2KOH+H2������ԭ������ȣ���ⷨ������Ϊ?��
2KMnO4+2KOH+H2������ԭ������ȣ���ⷨ������Ϊ?��
��4�������Ƶζ�������������ش��Ȳ������£�
�� ��ȡ0.80 g���ҵĸ�����ز�Ʒ�����50 mL��Һ��
�� ȷ��ȡ0.2014 g�����Ѻ�ɵ�Na2C2O4��������ƿ�У�������������ˮʹ���ܽ⣬�ټ������������ữ��
�� ��ƿ����Һ���ȵ�75��80 �棬�����â������Ƶĸ��������Һ�ζ����յ㡣��¼���ĸ��������Һ�����������ó���Ʒ���ȡ�
�ٵζ������з�Ӧ�����ӷ���ʽΪ?��
�ڴﵽ�ζ��յ�ı�־Ϊ?��
�ۼ����¶ȴ���90�棬���ֲ��ᷢ���ֽ⣬�ᵼ�²�ò�Ʒ����?�����ƫ�ߡ�����ƫ�͡�����Ӱ�족��?
�ܽ�һ�������������Һ���ữ�IJ�������Һ��ϣ���÷�ӦҺ��Mn2+��Ũ���淴Ӧʱ��t�ı仯��ͼ����ԭ�����Ϊ?��
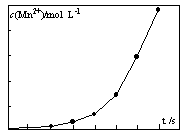
�ο��𰸣���1��c d��2������K2SO4�ܽ��С���ή�Ͳ�Ʒ�Ĵ��ȡ�������л�ԭ�ԣ��ᱻ���������Ͳ�Ʒ��������3��K2MnO4�е���Ԫ�ؿ�����ȫת����KMnO4�У���������ʡ���4����2MnO4�D+5C2O42?�D+16H+=2Mn2++10CO2��+8H2O ��MnO4�D+5H2C2O4+6H+=2Mn2++10CO2��+8H2O����ƿ����Һͻ��Ϊdz��ɫ�Ұ�����ڲ���ɫ����ƫ�ߣ�1�֣������ɵ�Mn2+������������Mn2+Ũ�����ӣ���Ӧ����Խ��Խ�졣
�����������1�����С���������������ʱ��Ӧѡ������������ǯ�� c����������d�������ǡ���2�����ݱ��е�����K2CO3���ܽ����K2SO4��10��������ʱ����K2SO4�ܽ��С��������ƽ�����ƣ��ή�Ͳ�Ʒ�Ĵ��ȡ�����������л�ԭ�ԣ��ᱻ����������������Ͳ�Ʒ��������3����ԭ������ȣ���ⷨ������ΪK2MnO4�е���Ԫ�ؿ�����ȫת����KMnO4�У���������ʡ���C2O42?�D�л�ԭ�Ա������������Ϊ������̼����������Һ�и�����صĻ�ԭ�����Ƕ��������ӣ��ζ������з�Ӧ�����ӷ���ʽΪ��2MnO4�D+5C2O42?�D+16H+=2Mn2++10CO2��+8H2O ��MnO4�D+5H2C2O4+6H+=2Mn2++10CO2��+8H2O�������ڸ����������ɫ��Һ������ͨ��������ɫ�ı仯��Ϊ�յ��жϣ���ƿ��һ��ʼ����ɫ��Һ���ﵽ�ζ��յ�ı�־Ϊ��ƿ����Һͻ��Ϊdz��ɫ�Ұ�����ڲ���ɫ�������ڲ��ᷢ���˷ֽ⣬Ũ����Ȼ��С���ⶨ�������϶������࣬�����������ص������ᵼ�²�ò�Ʒ����ƫ�ߡ��ܴ�ͼ���п��Կ��������ӵ�Ũ�ȵ��������ӳ̶Ƚϴ���ԭ�����Ϊ���ɵ�Mn2+������������Mn2+Ũ�����ӣ���Ӧ����Խ��Խ�졣
�����Ѷȣ�һ��
5��ѡ���� �����Ƕ�ijˮ��Һ�������Ӽ���ķ����ͽ��ۣ�������ȷ���ǣ�?��
A������NaOH��Һ�����ȣ�����ʹʪ�����ɫʯ����ֽ�������壬��ԭ��Һ��һ����NH4+
B������������CaCl2��Һ�������˰�ɫ��������Һ��һ���д�����CO32��
C���ýྻ�IJ�˿պȡ������Һ�����ڻ��������գ�����ɫ�ܲ����ܹ۲쵽�������ɫ������Һ��һ�����м����ӣ����ܺ���������
D���ȼ����������Ὣ��Һ�ữ���ټ�AgNO3��Һ�������˰�ɫ��������Һ��һ�����д�����Cl��
�ο��𰸣�C
���������A����������ˮ�Լ��ԣ�Ӧ��ʹʪ��ĺ�ɫʯ����ֽ����������B������������CaCl2��Һ�������˰�ɫ��������Һ�в�һ���д�����CO32���������ܺ����������������C���ýྻ�IJ�˿պȡ������Һ�����ڻ��������գ�����ɫ�ܲ����ܹ۲쵽�������ɫ������Һ��һ�����м����ӣ����ܺ��������ӣ���ȷ��D�������Ὣ��Һ�ữ�������������ӣ�����ȷ��ԭ��Һ��һ�����������ӣ�Ӧ�������ữ������
�����Ѷȣ�һ��