1、选择题 114号元素的一种同位素是由俄罗斯科学家合成的,存在时间只有30s,其质量数为289,该原子的中子数与电子数之差为
A.61
B.114
C.175
D.289
参考答案:A
本题解析:根据质量数=质子数+中子数,可得中子数为289-114=175,质子数=电子数=114,可得中子数与电子数只差为175-114=61,选A。
本题难度:一般
2、填空题 (16分)(Ⅰ)某元素的原子序数为33,写出该元素原子的核外电子排布式 ??,此元素的原子中被电子占据的轨道有?个,有 ??个能级(能量不同的轨道);
(Ⅱ)有五种元素A、B、C、D、E,A2+的电子层结构为1S22S22P63S23P63d5,B原子的M层为最外层且有两个未成对电子,C原子的L电子层的P轨道上有一个空轨道,D原子的L电子层的P轨道上只有一对成对电子,E原子的M电子层的P轨道半充满。写出A---E各元素的符号:A ??、B?、C?、D?、E?
参考答案:(Ⅰ) 1S22S22P63S23P63d104S24P3 ?,17个,8个;
(Ⅱ)A ?Mn、B S或Si 、C? C?、D? O?、E? P?
本题解析:(Ⅰ)根据核外电子排布规律可以写出33号元素的核外电子排布式为1S22S22P63S23P63d104S24P3,该元素原子中被电子占据的轨道,s轨道有4个,p轨道有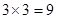 个,d轨道有5个,所以占据的轨道总共有18个,所给参考答案有误。该原子电子占据的能级有1S、2S、2P、3S、3P、3d、4S、4P总共有8个。
个,d轨道有5个,所以占据的轨道总共有18个,所给参考答案有误。该原子电子占据的能级有1S、2S、2P、3S、3P、3d、4S、4P总共有8个。
(Ⅱ)A2+的电子层结构为1S22S22P63S23P63d5,可以得出A2+的电子数目为23个,所以A原子的电子数目为25,所以A元素为25号元素Mn,B原子的M层为最外层且有两个未成对电子所以B原子的核外电子排布为1S22S22P63S23P2或1S22S22P63S23P4,所以B元素可能为S或Si,
C原子的L电子层的P轨道上有一个空轨道所以C原子的核外电子排布为1S22S22P2,所以C元素为C,D原子的L电子层的P轨道上只有一对成对电子可以得出D原子的核外电子排布为1S22S22P4,所以D元素为O,,E原子的M电子层的P轨道半充满E元素原子的核外电子排布为1S22S22P63S23P3,所以E元素为P。
本题难度:一般
3、选择题 下列关于硫酸的说法不正确的是
A.是化合物
B.是氧化物
C.是含氧化物
D.是含氧酸
参考答案:B
本题解析:分析:硫酸在水中电离出的阳离子只有氢离子属于酸;硫酸中含有氧元素,所以属于含氧酸;硫酸是由氢、氧、硫元素组成的纯净物,属于化合物.
解答:A、硫酸是由氢、氧、硫元素组成的纯净物,属于化合物,故A正确;
B、硫酸中含有氧元素,还含有H、S两种元素,氧化物中只含有两种元素,并且其中一种是氧元素的化合物,故B错误;
C、硫酸中含有氧元素,属于化合物,是含氧化合物,故C正确;
D、硫酸在水中电离出的阳离子只有氢离子属于酸,硫酸中含有氧元素,所以属于含氧酸,故D正确.
故选B.
点评:本题考查学生酸、汉阳算、含氧化合物、氧化物的概念知识,可以根据教材知识来回答,较简单.
本题难度:困难
4、填空题 有机物A~F之间的转化关系如下图所示(部分产物已略去),其中B的相对分子质量是D的2倍。

提示: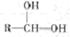 会自动脱水形成R―CHO
会自动脱水形成R―CHO
根据以上信息回答下列问题:
(1)B的分子式是?
(2)检验D中官能团可使用的试剂名称是?,写出D的相邻同系物与该试剂反应的化学方程式_______________________________。
(3)C遇FeCl3溶液显紫色,核磁共振氢谱中有四个峰,其峰面积比为1:2:2:1。写出C的结构简式_______________________。
(4)写出符合下列条件的C的同分异构体的结构简式_______、______、______、________。
①苯环上存在对位取代基;②遇FeCl3溶液显紫色;
③能与银氨溶液反应。
(5)写出A的结构简式__________________________。
(6)若1molA 和足量NaOH反应,最多能消耗___________mol NaOH。
和足量NaOH反应,最多能消耗___________mol NaOH。
参考答案: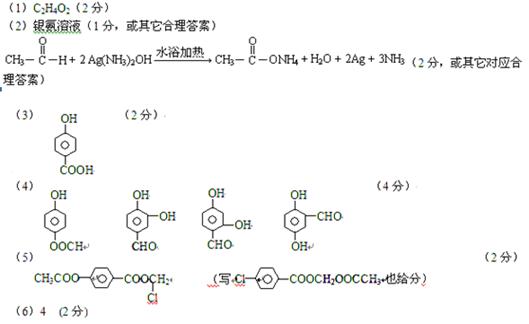
本题解析:略
本题难度:一般
5、选择题 X、Y、Z三种短周期元素在周期表中的位置如图所示,Y原子的最外层电子数是次外层电子数的3倍,下列说法正确的是

A.气态氢化物的沸点:Z<Y
B.Z元素的氧化物对应的水化物一定是一种强酸
C.三种元素原子半径的大小顺序为: X>Y>Z
D.Z单质与Fe反应生成的化合物中,铁元素显+3价
参考答案:A
本题解析:根据短周期元素在周期表中的相对位置可知,Y和X应该是第二周期元素。Y原子的最外层电子数是次外层电子数的3倍,实验Y应该是氧元素,则X是氮元素,Z是S元素。A、由于水分子间存在氢键,所以水的沸点高于H2S的沸点,A正确;B、硫酸是强酸,但亚硫酸是弱酸,B不正确;C、同周期自左向右原子半径逐渐减小,同主族自上而下原子半径逐渐增大,所以三种元素的原子半径大小顺序是Z>X>Y,C不正确;D、硫与铁化合生成的是氯化亚铁FeS,得不到+3价铁,D不正确,答案选A。
本题难度:一般