| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学知识点讲解《电解质和非电解质》练习题(六)
参考答案:A 本题解析:B中CH3COOH是弱电解质;C中NH3・H2O是弱电解质;D中HClO是弱电解质。 本题难度:一般 2、填空题 根据要求回答下列各题 |
参考答案:(共12分,每空1分)(Ⅰ)(1)④⑤⑥( 2)②⑦(3)④⑤(4)①③(Ⅱ)①2NaOH+CO2+H2O=2NaHCO3或NaOH+CO2=NaHCO3 ② MgCl2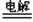 Mg+Cl2↑③ Fe2O3+2Al
Mg+Cl2↑③ Fe2O3+2Al 2Fe+Al2O3 ④ AgNO3+HCl=HNO3+AgCl(合理就给分)(Ⅲ).1:4 4:1 3:20 ; (Ⅳ)B
2Fe+Al2O3 ④ AgNO3+HCl=HNO3+AgCl(合理就给分)(Ⅲ).1:4 4:1 3:20 ; (Ⅳ)B
本题解析:(Ⅰ)电解质和非电解质都是化合物,从这个前提下进行分析,则答案为(1)④⑤⑥( 2)②⑦ (3)④⑤ (4)①③ 。(Ⅱ)联系平时所学的基础知识,完成化学方程式如答案所示。(Ⅲ).同温同压条件下,同体积的CH4和SO2的物质的量相同,则其质量之比是摩尔质量之比,则为1:4 ;同质量的CH4和SO2的体积之比是其摩尔质量的反比。若两者所含原子个数总数相等,假设都为1mol转化为CH4和SO2的质量之比是3:20 。(Ⅳ)a是电解池,b为原电池,在a中相当于电解水,在铁棒上氢离子放电,周围呈碱性,后者是吸氧腐蚀,在碳棒周围会生成氢氧根,因此首先观察到溶液变红的区域是Ⅰ和Ⅳ附近。
考点:本题考查了给定条件下化学反应方程式的书写和电化学反应原理。
本题难度:困难
3、选择题 下列物质中属于纯净物、化合物、盐、钙盐的是
A.CaO
B.Ca(OH)
C.CaCO3
D.CH4
参考答案:C
本题解析:A、CaO是纯净物、化合物,但不是盐,属于氧化物,错误;B、氢氧化钙是纯净物、化合物,但属于碱,错误;C、碳酸钙是纯净物、化合物,属于盐且是钙盐,正确;D、甲烷是纯净物、化合物,不属于盐,错误,答案选C。
考点:考查对物质分类的判断
本题难度:一般
4、填空题 (10分)现有下列十种物质:①H2 ②铝 ③CuO ④CO2 ⑤H2SO4 ⑥Ba(OH)2 ⑦红褐色的氢氧化铁液体 ⑧氨水 ⑨稀硝酸
⑩Al2 (SO4)3
(1)按物质的分类方法填写表格的空白处:
| 分类标准 | | 氧化物 | | | 电解质 |
| 属于该类的物质 | ② | | ⑧⑨ | ⑦ | |
参考答案:(10分)(1)
分类标准
金属单质
氧化物
溶液
胶体
电解质
属于该类的物质
②
③④
⑧⑨
⑦
③⑤⑥⑩
(2)Ba(OH)2+2HNO3=Ba(NO3)2+2H2O
(3)Al2(SO4)3= 2Al3++3SO42-, 9.03×1022, 0.6mol/L。
(4)Ba(OH)2+CO2=BaCO3↓+H2O。
本题解析:考查物质的分类及有关化学用语的书写。
(1)铝是金属单质。由两种元素组成的,其中一种是氧元素的化合物是氧化物,所以属于氧化物的是③④;氨水和稀硝酸都是溶液;红褐色的氢氧化铁液体属于胶体;溶于水或熔融状态下,能自身电离出阴阳离子的化合物是电解质,属于属于电解质的是③⑤⑥⑩。
(2)氢氧化钡是强碱,硝酸是强酸,二者发生中和反应,反应的化学方程式是Ba(OH)2+2HNO3=Ba(NO3)2+2H2O。
(3)硫酸铝是电解质,完全电离,所以电离方程式是Al2(SO4)3= 2Al3++3SO42-;17.1g硫酸铝的物质的量是17.1g÷342g/mol=0.05mol,所以根据电离方程式可知,含有的SO42-的粒子数为0.05mol×3×6.02×1023/mol=9.03×1022;SO42-的物质的量浓度为0.15mol÷0.25L=0.6mol/L。
(4)少量的CO2和氢氧化钡溶液反应生成的是碳酸钡白色沉淀和水,反应的方程式是Ba(OH)2+CO2=BaCO3↓+H2O。
本题难度:一般
5、选择题 下列状态的物质,既能导电又属于电解质的是
A.KNO3晶体
B.NaCl溶液
C.液态HCl
D.熔融的KOH
参考答案:D
本题解析:
试题解析:KNO3晶体没有自由移动的离子,故不导电;在水溶液中能电离出自由移动的硝酸根离子和钾离子,能导电,是电解质,故A错误;虽然氯化钠溶液能导电,但氯化钠溶液是混合物不是化合物,故B错误;液态氯化氢是电解质但不能导电,故C错误;熔融的氢氧化钾是能导电的电解质,故D正确.
考点:电解质的概念
本题难度:一般
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高中化学知识点归纳《反应热计算.. | |