1、选择题 工业制ClO2的化学反应:2NaClO3+SO2+H2SO4=2ClO2+2NaHSO4,下列说法正确的是
A.NaClO3在反应中化合价降低,失去电子
B.SO2在反应中发生氧化反应
C.1mol氧化剂在反应中得到2mol电子
D.H2SO4 在反应中作氧化剂
参考答案:
本题解析:
本题难度:困难
2、填空题 利用化合价推测物质的性质是化学研究的重要手段。
(1)从化合价的角度可以预测物质的性质。
①SO2的性质________________(填序号,下同)
A.只有氧化性 B.只有还原性 C.既有还原性又有氧化性
②SO2通入酸性KMnO4溶液中,溶液由紫色褪至无色。反应后,锰元素被还原成Mn2+,写出上述反应的离子方程式_________________________________
(2)Fe(OH)2很不稳定,露置在空气中容易被氧化,发生反应的离子方程式为__________________________________________________为了获得白色的Fe(OH)2沉淀,可以用不含Fe3+的FeSO4溶液与不含O2的蒸馏水配置的NaOH溶液反应制备。
①用硫酸亚铁晶体配置上述硫酸亚铁溶液时,还需加入_________来防止Fe2+被氧化
②除去蒸馏水中溶解的O2常采用_______的方法
(3)检验Fe3+的方法:_______________________(写出加入试剂的化学式和现象与结论)
参考答案:(1)①C②5SO2+2MnO4-+2H2O=4H++2Mn2++5SO42-(2)4Fe(OH)2+O2+2H2O=4Fe(OH)3①铁粉②加热煮沸(3)取少量溶液置于试管中,滴加几滴KSCN溶液,溶液变红,说明有Fe3+的存在。
本题解析:(1)①SO2中的S化合价是+4价,处于中间价态,既具有还原性又有氧化性,C正确;②SO2具有还原性,酸性KMnO4具有强氧化性,SO2被氧化成SO42-,+7价的Mn被还原成Mn2+,根据反应前后所带电荷数守恒及溶液是酸性,H2O作为反应物,H+作为生成物,因此离子方程式:5SO2+2MnO4-+2H2O=4H++2Mn2++5SO42-;(2)Fe(OH)2容易被氧气氧化成Fe(OH)3,4Fe(OH)2+O2+2H2O=4Fe(OH)3;①因为Fe+2Fe3+=3Fe2+,因此加入少量的铁粉来防止Fe2+被氧化;②溶解在水中的气体,往往采用加热煮沸法处理;(3)检验Fe3+存在,用KSCN溶液进行检验。
考点:考查氧化还原方程式的书写、铁的化合物的性质等相关知识。
本题难度:一般
3、选择题 下列反应中,既属于氧化还原反应同时又是放热反应的是
A.酸碱中和反应
B.Ba(OH)2.8H2O与NH4Cl
C.灼热的炭与CO2反应
D.甲烷与O2的燃烧反应
参考答案:D
本题解析:试题分析:首先判断哪些属于氧化还原反应:C项 和D项。放热反应的有A、D,故既属于氧化还原反应同时又是放热反应的是D项,答案选D。
考点:氧化还原反应和放热反应的判断
点评:本题综合考查氧化还原反应知识和化学反应的能量变化的判断,属于基础题,侧重培养学生的判断能力。
本题难度:困难
4、选择题 室温时将PH=5的硫酸溶液稀释1000倍后,则c(H+):c(SO42-)是
A.2:1
B.21:1
C.20:1
D.22:1
参考答案:C
本题解析:
本题难度:一般
5、选择题 白磷与氧可发生如下反应:P4+5O2===P4O10.已知断裂下列化学键需要吸收的能量分别为:P―P a kJ/mol、P―O b kJ/mol、P==="O" c kJ/mol、O==="O" d kJ/mol.根据右图所示的分子结构和有关数据估算该反应的ΔH,其中正确的是
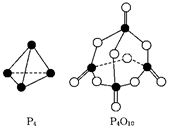
A.(4c+12b-6a-5d) kJ/mol
B.(6a+5d-4c-12b) kJ/mol
C.(4c+12b-4a-5d) kJ/mol
D.(4a+5d-4c-12b) kJ/mol
参考答案:B
本题解析:反应热就是断键吸收的能量和形成化学键所放出的能量的差值,所以根据物质的结构可知,该反应的反应热△H=(6a+5d-4c-12b) kJ/mol,答案选B。
本题难度:简单