1������� ��6�֣�CO��NO��SO2�������Ǵ�����Ⱦ�
��1��SO2����������Ⱦ�������������ڴ����о�����������ˮ�����������γ�Σ����������꣬��Ӧ�Ļ�ѧ����ʽ�ǣ���??��?��
��2��CO��NO������β������Ҫ�ɷ�֮һ��ұ���ķ���֮һ������������������װһ������ת������(�ò����ٺϽ�������)�������ص���ʹCO��NO��Ӧ�����ɿɲ��������̬����ѭ���������壬д��һ����̼��һ��������Ӧ�Ļ�ѧ����ʽ��?��
�ο��𰸣���1����2SO2+O2===2SO3����SO3+H2O=H2SO4��
(2) 2CO��2NO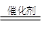 2CO2��N2
2CO2��N2
�����������1��SO2���л�ԭ�ԣ����Ա���������������������������������ˮ�������ᣬ��ӦʽΪ2SO2+O2===2SO3��SO3+H2O=H2SO4��
��2�����������̬����ѭ�����������й���CO2����˵��NO����ԭ���ɵ��ǵ�������ӦʽΪ2CO��2NO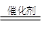 2CO2��N2��
2CO2��N2��
�����Ѷȣ�һ��
2��ѡ���� Cl2ͨ��������Һ�У��ܷ����û���Ӧ���ǣ�������
A��HCl
B��NaCl
C��NaBr
D��KNO3
�ο��𰸣�������HCl��NaCl�Լ�KNO3������Ӧ������NaBr������Cl2+2NaBr�T2NaCl+Br2��Ϊ�û���Ӧ��
��ѡ��C��
���������
�����Ѷȣ���
3��ѡ���� ������������ͨ��30mLŨ��Ϊ10��0mol/L����������Ũ��Һ�У���������ʱ�����Һ���γ�NaCl��NaClO��NaClO3�Ĺ�����ϵ�������ж���ȷ����
A����NaOH��Ӧ������һ��Ϊ0��15 mol
B������Ӧ�б���������Ԫ�غͱ���ԭ����Ԫ��֮��Ϊ1:4ʱ����Һ��NaClO��NaClO3�����ʵ���֮��Ϊ3:1
C����Һ��n(Na��):n(Cl��)����Ϊ7:3
D����Cl2��NaOH�ķ�Ӧ��ת�Ƶĵ���Ϊn mol����0��15��n��0��35
�ο��𰸣�A
���������A����������֪������������ͨ��30mLŨ��Ϊ10��0mol/L����������Ũ��Һ�У�����������ȫ��Ӧ������Ԫ���غ�֪��2n��Cl2��=n��NaOH��=n��NaCl��+n��NaClO��+n��NaClO3��=0.03L��10mol/L=0.3mol��n��Cl2��=0.15mol����ȷ��B�����ݵ����غ�֪������Ӧ�б���������Ԫ�غͱ���ԭ����Ԫ��֮��Ϊ1:4ʱ����Һ��NaClO��NaClO3�����ʵ���֮��Ϊ1:3������C������Cl2+2NaOH=NaCl+NaClO+H2O��3Cl2+6NaOH=5NaCl+NaClO3+3H2O��֪����������ֻ��NaClO��n��Na+����n��Cl-�����Ϊ2��1������������ΪNaClO3��n��Na+����n��Cl-����СΪ6��5����Һ��n(Na��):n(Cl��)������Ϊ7:3������D�����ݷ���ʽCl2+2NaOH=NaCl+NaClO+H2O��3Cl2+6NaOH=5NaCl+NaClO3+3H2O��֪����������ֻ��NaClO��ת�Ƶ��������٣�Ϊ0.15mol����������ֻ��NaClO3��ת�Ƶ�������࣬Ϊ0.25mol������
�����Ѷȣ�һ��
4��ѡ���� �����й�Cl��N��S��Si�ȷǽ����������˵������ȷ���ǣ�?��
A���轺��Ũ���ᡢ��ʯ�ҡ���ˮ�Ȼ��ƶ���ʵ���ҳ��õĸ���������Ƕ�������������NH3��Cl2��SO2��H2������
B����������ʯ�����Ͽ���Ư�ۣ�����Ч�ɷ����Ȼ���
C������һ�����õİ뵼����ϣ������������غͼ����оƬ
D��Һ�������������
�ο��𰸣�AB
�����������ˮ�Ȼ��Ʋ����Ը���NH3Ũ����Ҳ�����Ը���NH3��A����������ʯ�����Ͽ���Ư�ۣ�����Ч�ɷ��Ǵ�����ƣ�B����
�����Ѷȣ�һ��
5��ѡ���� �������ᡢ���ᡢ���������������
A�����߶���ǿ�ᣬ��ϡ��Һ��ֻ��ϡ������ͭ�ڳ��·�Ӧ
B��Ũ�� ����������Ũ����ʹֽ�ű�ڣ�Ũ���᳣����ͭ��Ӧ����������
����������Ũ����ʹֽ�ű�ڣ�Ũ���᳣����ͭ��Ӧ���������� �ߵ�ǿ������
�ߵ�ǿ������
C����ǿ�����Ե�Ũ������Ũ���ᰴ������Ͽ��Եõ������Ը�ǿ����ˮ
D�������������Ũ�����Ũ����Ķۻ����ڻ�ѧ��Ӧ
�ο��𰸣�BC
�����������
�����Ѷȣ�һ��