1、填空题 现需配制0.2mol/LNaHCO3?溶液450mL,某同学如图转移溶液.
①图中的错误是______
②实验中应选择容量瓶的规格是______(选填100mL或500mL);实验时需称取NaHCO3的质量为______g
③配制时,其正确的操作顺序是______(字母表示,每个字母用且只能用一次).
A、每次用30mL水洗涤烧杯2~3次,洗涤液均注入容量瓶
B、准确称取计算量的固体于烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其充分溶解
C将溶解后的溶液沿玻璃棒注入容量瓶中
D、将容量瓶盖紧,振荡,摇匀
E、改用胶头滴管加水,使溶液凹面恰好与刻度线相切
F、继续往容易瓶内小心加水,直接液面接近刻度2~3cm处.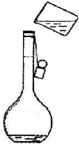
参考答案:①转移溶液需要玻璃棒引流,否则会使溶液溅出而导致配制溶液浓度偏低,故答案为:未用玻璃棒引流;
②实验室没有450mL容量瓶,选取的容量瓶规格应该等于或稍大于需要配制溶液的体积,所以应该选取500mL的容量瓶,m=CVM=0.2mol/L×0.5L×84g/mol=8.4g,故答案为:500mL;8.4;
③配制时,一般可分为以下几个步骤:计算、称量、溶解、冷却、转移、洗涤、定容、摇匀,所以其操作步骤的正确顺序为BCAFED,故答案为:BCAFED.
本题解析:
本题难度:一般
2、选择题 将50g浓度为18.4mol/L、密度为1.84g/cm3的某硫酸稀释成9.2mol/L的溶液.则加入水的体积(水的密度为1.0g/cm3)
A.小于50ml
B.等于50ml
C.大于50ml
D.等于ml
参考答案:A
本题解析:分析:令浓硫酸的体积为VmL,根据稀释定律计算稀释后溶液的体积,硫酸溶液的浓度越大密度越大,据此判断稀释后溶液的质量,进而判断加入水的质量,再根据V=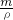 判断.
判断.
解答:令浓硫酸的体积为VmL,根据稀释定律,稀释前后溶质硫酸的物质的量不变,设稀释后溶液的体积为a,
则:VmL×18.4mol/L=a×9.2mol/L,解得a=2VmL,
硫酸溶液的浓度越大密度越大,所以稀释后硫酸的密度小于1.84g/cm3,故稀释后硫酸的质量小于100g,所以加入水的质量小于100g-50g=50g,
故加入水的体积小于 =50mL,
=50mL,
故选A.
点评:本题考查物质的量浓度的有关计算,难度中等,清楚硫酸溶液的浓度越大密度越大是解题关键.
本题难度:简单
3、选择题 用NaCl固体配制0.1mol?L-1的NaCl溶液,下列操作或说法正确的是( )
A.将5.85g NaCl固体溶于1?L水中可配成0.1?mol?L-1的NaCl溶液
B.称量时,将固体NaCl直接放在天平左盘上
C.固体溶解后,将溶液转移到容量瓶中,然后向容量瓶中直接加水稀释到刻度线
D.配制溶液时容量瓶中原来有少量蒸馏水不会影响实验结果
参考答案:D
本题解析:
本题难度:简单
4、简答题 实验室需要250mL0.5mol/L的稀硫酸溶液,现用密度为1.84g/mL,质量分数为98%浓硫酸配制;填空并请回答下列问题:
(1)请先通过计算(要有计算过程),再确定量取______mL浓硫酸.
(2)下列仪器中,不会用到的是______
A.250mL容量瓶;B.500mL容量瓶;C.托盘天平;D.10mL量筒;E.玻棒;
(3)若要实施配制,除上述仪器外,尚缺的仪器或用品是______.
(4)容量瓶在使用前必须进行的操作是______.
(5)配制过程简述为以下各步:其正确的操作顺序为______(填各步骤序号).A.冷却;B.洗涤;C.量取;D.溶解;E.定容;F.摇匀;G.移液
(6)在配制过程中,定容时若俯视刻度线,则所配溶液的浓度偏______(填“高”或“低”);若在滴加蒸馏水时,不慎超过了刻度线,应如何处理?______.
参考答案:(1)配制250mL 0.5mol/L的稀硫酸,需要硫酸的物质的量是:0.25L×0.5mol/L=0.125mol,设需要密度为1.84g/mL,质量分数为98%浓硫酸溶液的体积为VmL,根据溶液的稀释可得:V×1.84×98%98mol=0.125mol,解得V≈6.8mL,
故答案是:6.8mL;
(2)配制250mL稀硫酸溶液,需要用到的仪器有:250mL容量瓶、10量筒、玻璃棒、胶头滴管等,所以用不到的是:B.500mL容量瓶、C.托盘天平,
故答案是:BC;
(3)若要实施配制,除上述仪器外,定容的时候需要胶头滴管,稀释时需要用到烧杯,
故答案是:胶头滴管、烧杯;
(4)容量瓶在使用前必须进行检查是否漏水,
故答案是:查漏;
(5)配制一定物质的量浓度的溶液的步骤是:计算、量取、稀释、冷却、移液、洗涤、定容、摇匀,所以正确顺序是CDAGBEF,
故答案是:CDAGBEF;
(6)定容是俯视容量瓶的刻度线,会使配制的溶液的体积偏小,所配制的溶液的浓度偏高;定容时若是加蒸馏水超过了容量瓶的刻度线,不能用胶头滴管吸出,必须重新配制溶液,
故答案是:高;重新配制溶液.
本题解析:
本题难度:一般
5、实验题 实验室配制500 mL 0.2 mol/L的FeSO4溶液,实际操作步骤有:
①在天平上称量一定量的绿矾(FeSO4・7H2O),放入烧杯,加水溶解;
②把制得的溶液小心地注入500 mL容量瓶中;
③继续向容量瓶中加水至距刻度1~2cm处,改用胶头滴管加水至刻度线;
④用少量水洗涤烧杯和玻璃棒2~3次,每次将洗涤液转入容量瓶,并摇匀;
⑤将容量瓶塞塞紧,充分摇匀。
填写下列空白:
(1)称量绿矾的总质量是_____________g。
(2)操作步骤的正确顺序是(填序号)____________。
(3)本实验使用到的仪器是__________________________。
(4)若没有进行④操作,会使结果(填偏高、偏低、无影响,下同)__________;若用天平称固体时,砝码上沾有油污,则所配制的溶液浓度将__________;若定容时加水至凹面的最高点与刻度线相平,则所配制的溶液浓度将__________。
(5)在进行②操作时,不慎有液体溅出,应该怎样处理?______________________。
参考答案:(1)27.8
(2)①②④③⑤
(3)天平、烧杯、玻璃棒、胶头滴管、500 mL容量瓶、药匙
(4)偏低;偏高;偏高
(5)重新按正确的方法、步骤配制
本题解析:
本题难度:一般