1、选择题 Na2CO3固体中可能含有杂质K2CO3、NaHCO3、NaCl中一种或几种,取10.6g样品,加入足量的稀盐酸产生气体4.8g,下列分析正确的是
A一定含有NaHCO3?B一定含有K2CO3
C一定不含NaCl ?D一定含有NaCl
参考答案:A
本题解析:略
本题难度:一般
2、计算题 已知K2O2与CO2的反应类似Na2O2与CO2的反应。
某潜艇要执行水下任务,共25位船员,大概每人每天需耗氧1.6 kg,如果船载K2O2 2.75 t作为供氧剂,潜艇最多能下潜几天?
参考答案:潜艇最多能下潜10天。
本题解析:2K2O2+2CO2====2K2CO3+O2
2×110 kg? 32 kg
2.75×103 kg? x
x=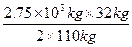 ="400" kg
="400" kg
25位船员每天共需O2:25×1.6 kg="40" kg,故可下潜10天。
本题难度:简单
3、填空题 钠是活泼金属的代表,钠和钠的化合物是中学化学的基础知识。请回答下列有关问题。
(1)钠跟水剧烈反应,生成?和氢气(H2),此实验说明钠的化学性质活泼;
(2)钠有两种氧化物,其中能用于呼吸面具和潜水艇中作为氧气来源的氧化物是:
?;
(3)固体碳酸钠中含有碳酸氢钠杂质,除去此杂质的简单方法是?(填“萃取”或“加热”或“蒸馏”)。
参考答案:(1)NaOH或氢氧化钠;(2)Na2O2或过氧化钠;(3)加热
本题解析:(1)钠跟水剧烈反应,生成氢氧化钠和氢气。
(2)钠的氧化物有氧化钠和过氧化钠,其中能用于呼吸面具和潜水艇中作为氧气来源的氧化物是过氧化钠。
(3)碳酸氢钠不稳定,加热分解生成碳酸钠、水和CO2,所以固体碳酸钠中含有碳酸氢钠杂质,除去此杂质的简单方法是加热。
点评:该题是基础性试题的考查,难度不大,该题的关键是记住钠及其化合物的性质并能灵活运用即可。
本题难度:一般
4、填空题 (6分)
(1)Na与水反应的化学方程式是:?。
(2) 由Al与Fe2O3组成的铝热剂常用于焊接铁轨。Al与Fe2O3混合强热反应的的化学方程式为:?。
参考答案:(1)2Na + 2H2O ="==" 2NaOH + H2↑(2)2Al + Fe2O3高温 2Fe + Al2O3
本题解析:(1)2Na + 2H2O ="2NaOH" + H2↑
(2)2Al + Fe2O3高温 2Fe + Al2O3
本题难度:简单
5、选择题 把2.1g的CO与H2组成的混合气体与足量的O2充分燃烧后,立即通入足量的Na2O2固体中,固体的质量增加
A.7.2g
B.3.6g
C.2.1
D.无法确定
参考答案:C
本题解析:物质燃烧生成CO2和水,然后被过氧化钠吸收生成碳酸钠、氢氧化钠和氧气,2CO2+2Na2O2=2Na2CO3+O2、2H2O+2Na2O2=4NaOH+O2↑。因此相当于固体Na2O2只吸收了CO2中的“CO”,H2O中的“H2”;可以看做发生相应的反应:Na2O2+CO===Na2CO3,Na2O2+H2===2NaOH(实际上两反应都不能发生)。因此凡分子组成符合(CO)m・(H2) n的物质,m g该物质在O2中完全燃烧,将其产物CO2和水蒸气?通过足量的Na2O2后,固体增重必为m g。或是由C、H、O三种元素组成的物质,只要C、O原子个数比为1∶1,即可满足该条件。中学阶段常见的符合这一关系的物质有:无机物:H2、CO及H2和CO的混合气体;有机物:CH3OH甲醇、HCHO甲醛、CH3COOH乙酸、HCOOCH3甲酸甲酯、C6H12O6葡萄糖。所以固体增加的质量就是2.1g,答案选C。
本题难度:一般