1��ѡ���� ��Na2O2Ͷ��FeCl2��Һ�У��ɹ۲쵽��������(? )
A�����ɰ�ɫ����
B�����ɺ��ɫ����
C�������ݲ���
D���ޱ仯
2�������� KOH��KHCO3����Ļ����25.6 g,��250 ���������,��ȴ������������ʧ��4.9 g��
(1)����ʼ�����İٷ���ɡ�
(2)��������������ʧ��Ϊ2.1 g,��ʱ��ʼ�����İٷ�������Ƕ���?
3������� ʵ��Ŀ�ģ�̽������������ˮ��Ӧ�����Һ�μӷ�̪��Һ�ȱ�����ɫ��ԭ��
����������롿
��1�����ݹ���������ˮ��Ӧ��ԭ����2Na2O2+2H2O�T4NaOH+O2�������������ƹ�����ȫ�ܽⷴӦ�����Һ�еμӷ�̪��Ӧֻ�����������ɫ����ʵ���з��ַ�̪��������ɫ���ɴ�������µIJ��룺
A��������Ư����
B������������Ư����
C��______
��ʵ�����жϡ�
����ɱ���
| ʵ���� | 1 | 2 | 3
ʵ��װ��
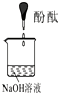
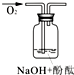
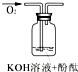
��֤����
______
C
______
ʵ������ | ��Һ������ɫ
ʵ��˵�� | 1��2��ʵ����NaOH��Һ����______����������ƹ��塱���������ƹ��塱�����������ƹ��塱������ˮ���Ƶģ�
|
��2����������ʵ��������֣�����������ˮ��Ӧ�����У���Ԫ���γ����ȶ��Ļ������Һ�л�������һ�ֲ����ȶ�������Ư���Ե�����X��X�Ļ�ѧʽ��______��
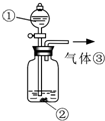
��3��������ͼװ�ö���Һ�в����ȶ������ʽ���̽�����ڢٴ�װ���������______����ѡ���ͬ�����ڴ�װ���������______��
A����̪�Լ�
B������������ˮ��Ӧ�����Һ
C����������
D���������ƹ������Ƶ���Һ
��4���������______������������ˮ��Ӧ�Ļ�ѧ����ʽû��д��X����ԭ����______��
4��ѡ���� ��һС������Ƴ���¶���ڿ����з���һϵ�б仯�����ղ����ǣ���?��
A��NaOH
B��Na2O
C��Na2O2
D��Na2CO3
5�������� agNa2CO3��NaHCO3�����������������ٵ�bg�������� ��NaHCO3����������Ϊ��?��
��NaHCO3������������?��