| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学必考知识点《物质的量》高频试题预测(2019年最新版)(八)
参考答案:B 本题解析:臭氧含有24个电子,标准状况下,2.24L臭氧是0.1mol,A正确;B中溶液的体积不一定是1L,不能减少溶液的浓度,B不正确;乙烯和丙烯的最简式是相同的,都是CH2,则42 g乙烯和丙烯的混合气体中含有的碳原子的物质的量是42g÷14g/mol=3mol,C正确;常温下水中氢离子的浓度是l×10-7mol/L,则1L水中含有的H+数为l×10-7NA,D正确,答案选B。 本题难度:困难 2、选择题 欲配制100ml 1.0 mol/L Na2SO4溶液,正确的方法是 参考答案:B 本题解析: 本题难度:简单 3、选择题 已知1.505×1023个X气体分子的质量为8 g,则X气体的摩尔质量是 |
参考答案:D
本题解析:1.505×1023个X气体分子的物质的量为1.505×1023/6.02×1023mol-1=0.25mol,则X气体的摩尔质量是8g/0.25mol=32g /mol ,答案选D。
考点:阿伏加德罗常数,摩尔质量
本题难度:一般
4、选择题 某无色溶液中含有H+、Al3+、Mg2+三种阳离子,逐滴加入0.1moL・L-1 NaOH溶液,消耗NaOH溶液体积(X轴)和生成沉淀(Y轴)之间的函数关系如下图所示,则溶液中H+、Al3+、Mg2+三种阳离子的物质的量浓度之比为(?)
A.1:1:1
B.2:2:1
C.2:1:1
D.1:1:2
参考答案:B
本题解析::①根据图象知,横坐标为0-10时发生的反应是:盐酸和氢氧化钠的反应 HCl+NaOH=NaCl+H2O,盐酸和氢氧化钠物质的量以1:1反应,由图象的横坐标知,氯离子的物质的量=盐酸的物质的量=氢氧化钠的物质的量=0.1mol/L×(0.010L-0)=0.001mol,即n(H+)=0.001mol;
②当横坐标的数值为60后,随着横坐标数值的增大沉淀的量逐渐减少,说明氢氧化铝和氢氧化钠反应生成了偏铝酸钠,所设n(Mg2+)=xmol,根据镁离子守恒知硫酸镁的物质的量为xmol,n(Al3+)=ymol,再根据铝离子守恒知,以横坐标为10-70时,发生的化学反应是:
2OH-+ Mg2+=Mg(OH)2 ↓
2mol ?1mol
2xmol ?xmol
3OH-+ Al3+=Al(OH)3↓
3mol 1mol ?1mol
3ymol? y? ymol
所以生成沉淀的质量为最大时,氢氧化钠的物质的量为(2x+3y)mol=0.1mol/L×(0.06-0.01)=0.005mol;
③当横坐标的数值为60-70时,沉淀的质量减少,说明氢氧化铝和氢氧化钠反应生成偏铝酸钠导致沉淀的质量减少.
所以发生的化学反应方程式为
Al(OH)3+NaOH=NaAlO2+2H2O
1mol ?1mol
ymol ?0.1mol/L×(0.07-0.06)L
y=0.001
(2x+y)mol=0.001mol,所以x=0.0005
故n(Mg2+)=xmol=0.001mol,n(Al3+)=ymol=0.001mol
在同一溶液中,各离子的物质的量浓度之比等于其物质的量之比,即n(H+):n(Mg2+):n(Al3+)=0.001mol:0.001mol:0.0005mol=2:2:1,故选B。
点评:本题考查了根据图象进行有关计算,能根据图象正确判断各拐点之间发生的化学反应是解本题的关键,难度中等。
本题难度:一般
5、选择题 科学家刚刚发现了某种元素的原子X,X原子的质量是ag。已知12C(含6个质子和6个中子的一种碳原子,相对原子质量为12)的原子质量是bg,nA是阿伏加德罗常数的值,下列说法正确的是
A.由已知信息可知:nA=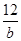
B.X原子的摩尔质量是nAa g/mol
C.Wg X原子的物质的量是 mol
mol
D.X原子的相对原子质量为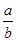
参考答案:AB
本题解析:
A、B正确;C、不正确,Wg X原子的物质的量是 mol ; D.不正确,X原子的相对原子质量为
mol ; D.不正确,X原子的相对原子质量为 。
。
本题难度:一般
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学知识点总结《磷及其化合.. | |