1、选择题 下列溶液中物质的量浓度为1mol/L的是
A.将40gNaOH 溶解在1L水中
B.将22.4LHCl气体溶于水配成1 L溶液
C.将1L 10 mol/L的浓盐酸加入9 L水中
D.将10 g NaOH溶解在少量水中,再加蒸馏水直到溶液体积为250 mL
参考答案:D
本题解析:根据c=n/V可知,选项A不正确,溶液的体积不是1L;选项B不正确,因为不一定是在标准状况下;选项C中,溶液的体积不是10L;因此正确的答案选D。
本题难度:一般
2、选择题 用已准确称量过的氯化钠固体配制1.00mol?L-1的氯化钠溶液0.5L,要用到的仪器是( )
①500mL容量瓶②试管③烧瓶④胶头滴管⑤烧杯 ⑥玻璃棒⑦托盘天平⑧药匙.
A.①④⑤⑥⑦⑧
B.①②④⑤
C.①④⑤⑥
D.全部
参考答案:操作步骤有称量、溶解、移液、洗涤、定容、摇匀等操作,一般用托盘天平称量,用药匙取药品,在烧杯中溶解,冷却后转移到500ml容量瓶中,并用玻璃棒引流,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,所以需要的仪器为:托盘天平、药匙、烧杯、玻璃棒、500ml容量瓶、胶头滴管,由于氯化钠已经称量完毕,故需要烧杯、玻璃棒、500ml容量瓶、胶头滴管,即①④⑤⑥,
故选C.
本题解析:
本题难度:简单
3、选择题 用NA表示阿伏加德罗常数的值,下列叙述正确的是
A.1mol CH3+(碳正离子)中含有电子数为10NA
B.常温常压下,17g NH3中含有原子数4NA
C.常温常压下,22.4 L水中含有的共价键数为2NA
D.在密闭容器中,1molN2与3molH2在一定条件下充分反应,生成氨气的分子数为2NA
参考答案:B
本题解析:A、1mol CH3+(碳正离子)中含有电子数为8NA,错误;B、常温常压下,17g NH3的物质的量为1mol,所以含有原子数4NA,正确;C、常温常压下,22.4 L水的质量为22400g,含有的共价键数大于2NA,错误;D、在密闭容器中,1molN2与3molH2在一定条件下充分反应,不可能完全转化为氨气,错误,答案选B。
本题难度:一般
4、计算题 氯化钠与氯化镁的混合物中,已知其钠离子与镁离子的物质的量之比为3:2。
(1)求混合物中两种物质的质量比。
(2)如果混合物中共有28 mol的Cl-,求混合物中氯化钠和氯化镁的质量各是多少?
参考答案:(1)根据NaCl、MgCl2的组成知,混合物中Na+与 Mg2+物质的量之比,亦为NaCl与MgCl2的物质的量之比。
∵n(NaCl)2 : n(MgCl2) =3:2
∴m(NaCl):m(MgCl2)=n(NaCl)・M(NaCl): n(MgCl2)・M( MgCl2)
=3mol×58.5g・mol-1:2mol×95g・mol-1 =351:380
(2)由Na+~Cl-,Mg2+~2Cl-得 n(Na+):n(Mg2+):n(Cl-)=3:2:(3+2×2)=3:2:7
当混合物中共有28 mol Cl-时, n( NaCl) = 28 mol×=12 mol,
n(MgCl2)=28mol×=8 mol.
则m(NaCl)=n(NaCl)・M(NaCl)=12mol×58.5 g.mol-1= 702 g
m(MgCl2)=n(MgCl2)・M(MgCl2)=8 mol×95 g.mol-1= 760 g
答:(1)混合物中氯化钠与氯化镁的质量比为351:380;
(2)如果混合物中共有28 mol Cl-,混合物中氯化钠的质量为702 g,氯化镁的质量为760 g。
本题解析:
本题难度:一般
5、填空题 将一种化学式为R(NO3)x・nH2O的硝酸盐晶体6.05 g溶于水配成500 mL溶液,用石墨棒作为电极材料对此溶液进行电解。当通过电流强度为5 A的电流16.05 min时,溶液中的金属离子已全部放电,且其中一电极增重1.60 g(已知此晶体的摩尔质量为242 g・mol-1)。
则:①x=____________,②R的相对原子质量为____________,③n=____________。
参考答案:①2?②64?③3
本题解析:已知“溶液中的金属离子已全部放电,且其中一电极增重1.60 g”,所以R的质量为1.60 g,晶体的物质的量为6.05 g/242 g・mol-1="0.025" mol。所以R的相对原子质量为:1.60/0.025=64。溶液中通过的电量为Q=It=5C/s×16.05 min×60 s/min=4.815×103 C,则电子的物质的量: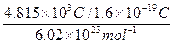 ="0.05" mol,则每个原子得2个电子,金属为+2价,x=2。n=(242-64-2×62)/18=3。
="0.05" mol,则每个原子得2个电子,金属为+2价,x=2。n=(242-64-2×62)/18=3。
点评:解答本题的思路是根据相关定义展开的。物质的相对原子质量在数值上等于其摩尔质量,所以要求R的相对原子质量需要找物质的质量和其物质的量。从定义出发,看似方法很笨,但是只要基础扎实,解题细心,一样可以很快地解出较难的试题。在高三复习中,应注意定义、概念,注重基础,重视课本,才能帮助自己提高能力,摆脱题海。
本题难度:简单