| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学知识点总结《物质的量》典型例题(二)
参考答案:D 本题解析:A、5.6g铁粉的物质的量是0.1mol,0.1mol铁粉在0.1mol氯气中充分燃烧,铁过量,氯气完全反应,转移电子数为0.2NA,A错误;B、Na2S和Na2O2摩尔质量相同,都是78g/mol,且化合物中阴阳离子的个数之比均是1:2;7.8g Na2S和Na2O2的混合物物质的量为0.1mol,含有的阴离子数0.1NA,B错误;C、浓硫酸与铜的反应中随着反应的进行,浓硫酸的浓度降低,而稀硫酸与铜不反应,所以50mL18.4mol/L浓硫酸与足量铜加热反应,生成SO2分子的数目小于0.46NA,C错误;D、NO2和N2O4的最简式相同,均是NO2,所以常温常压下,46g的NO2和N2O4混合气体中相当于含有NO2的物质的量是1mol,因此含有的原子数为3NA,D正确,答案选D。 本题难度:一般 2、选择题 在100g浓度为18mol/L、密度为ρ(g/cm3)的浓硫酸中加入一定量的水稀释成9mol/L的硫酸,则加入水的体积( ) |
参考答案:A
本题解析:硫酸的密度等于水的,根据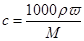 可知,当硫酸的浓度稀释成9mol/L时,溶液的质量分数大于原来的1/2,所以加入的水的质量小于100g,则体积小于100ml,答案选A。
可知,当硫酸的浓度稀释成9mol/L时,溶液的质量分数大于原来的1/2,所以加入的水的质量小于100g,则体积小于100ml,答案选A。
本题难度:一般
3、选择题 下列溶液中Cl-浓度最小的是( )
A.200mL2mol/LMgCl2溶液
B.1000mL2.5mol/LNaCl溶液
C.300mL5mol/LKClO3溶液
D.250mL1mol/LAlCl3溶液
参考答案:A、200mL2mol/LMgCl2溶液中氯离子的浓度为4mol/L;
B、1000mL2.5mol/LNaCl溶液中氯离子的浓度为2.5mol/L;
C、300mL5mol/LKClO3溶液不存在氯离子;
D、250mL1mol/LAlCl3溶液中氯离子的浓度为3mol/L.
故选:C.
本题解析:
本题难度:简单
4、选择题 下图锥形瓶中装满了c mol・Lˉ1的Na2SO4溶液,经测定其中含有a mol SO42-,则锥形瓶容积为
A.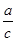 L
L
B.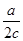 L
L
C.acL
D.2acL
参考答案:A
本题解析:根据C=n/V,硫酸钠溶液中SO42-的物质的量是amol,则Na2SO4溶液中硫酸钠的物质的量也是amol,所以该溶液的体积也是锥形瓶的容积为amol/cmol/L=a/cL,答案选A。
考点:考查溶液物质的量浓度的换算
本题难度:一般
5、选择题 某氯化镁溶液的密度为1.18g/cm3,其中镁离子的质量分数为5.1%,300mL该溶液中Cl-离子的物质的量约等于
[? ]
A. 0.37mol
B. 0.63mol
C. 0.74mol
D. 1.5mol
参考答案:D
本题解析:
本题难度:简单
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学试题《物质组成与性质实.. | |