1、选择题 类推的思维方法在化学学习中具有重要意义,但是类推的结论要经过实践的检验才能确定正确与否。下列几种类推结论中正确的是
A.甲苯能与酸性高锰酸钾溶液反应,所以苯也可以
B.SO2能与碱反应,所以非金属氧化物都能与碱反应
C.Al和S直接化合可得到Al2S3,所以Fe与S直接化合也可得到Fe2S3
D.某些盐的离子水解形成胶体可以做净水剂,明矾可做净水剂,所以FeCl3也可以
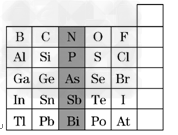
2、选择题 下图是元素周期表的一部分,下列说法正确的是?
[? ]
A.阴影部分元素在周期表中处于第ⅣA族
B.H3AsO4的酸性大于H3PO4
C.根据NaH的存在,也可把氢元素放在第ⅦA族
D.向硅酸钠溶液中加入盐酸可证明氯的非金属性强于硅
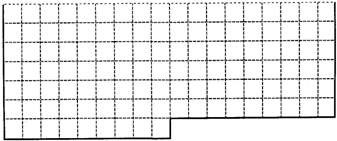
3、填空题 Ⅰ.上表中的实线是元素周期表部分边界,请在表中用实线补全元素周期表边界,并画出金属和非金属的分界线,用阴影画出铁元素所在的族.
Ⅱ.A、B、C、D、E都是短周期元素,原子序数依次增大,A、B处于同一周期,C、D、E同处另一周期.C、B可按原子个数比2:l和1:1分别形成两种离子化合物甲和乙.A原子的最外层电子数比次外层电子层多3个.E是地壳中含量最高的金属元素.根据以上信息回答下列问题:
(1)D元素在周期表中的位置是______,画出B元素简单离子结构示意图______,乙物质的电子式是______
(2)A、B、C、D、E五种元素的原子半径由小到大的顺序是(用元素符号填写)______
(3)E的单质加入到C的最高价氧化物对应的水化物的溶液中,发生反应的离子方程式是______
(4)简述比较D与E金属性强弱的实验方法:______
(5)E的单质、石墨和二氧化钛(TiO2)按比例混合,高温下反应得到的两种化合物均由两种元素组成,且都是新型陶瓷材料(在火箭和导弹上有重要应用)其反应方程式为______.
4、选择题 X、Y、Z、W四种元素在周期表中相对位置如图,Y、Z质子数之和为21,下列说法正确的是

[? ]
A.常压下,四种元素单质中,W单质的熔点最高
B.X的气态氢化物比Y的气态氢化物稳定
C.Z的阳离子与Y的阴离子电子层结构相同
D.W元素的金属性比Z元素金属性强
5、选择题 下列实验过程中,始终无明显现象的是
A.HCl通入Fe(NO3)2溶液中
B.CO2通入Ca(NO3)2溶液中
C.Cl2通入Na2SiO3溶液中
D.NH3通入Ca(HCO3)2溶液中