1、选择题 下列说法不正确的是( )
A.石油裂解、煤的气化、海水制镁、纤维素制硝酸纤维等过程中都包含化学变化
B.医疗上常用硫酸钡作X射线透视胃肠的“钡餐”
C.食用加碘盐可防治核辐射对人体的伤害
D.放射性同位素释放的射线可用于育种、治疗肿瘤
参考答案:C
本题解析:
本题难度:一般
2、选择题 短周期元素甲、乙、丙、丁、戊五种元素在元素周期表中的位置如下图所示,其中戊是同周期中原子半径最小的元素。下列有关判断正确的是

[? ]
A.最外层电子数:甲>乙>丙>丁>戊
B.简单离子的离子半径:丙<乙<戊<丁
C.含有丁元素的酸有多种
D.乙的氢化物多种多样,丙、丁、戊的氢化物各有一种
参考答案:C
本题解析:
本题难度:一般
3、填空题 分某化学兴趣小组为了探索铝电极在原电池中的作用,设计并进行了一系列实验,实验结果记录如下:
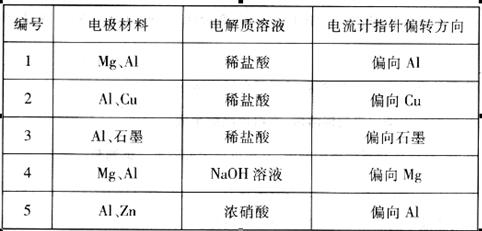
请根据上表中的实验记录回答下列问题:
(1)实验1、2中的Al所作的电极是否相同?____________________。
(2)在实验3中,Al作__________极,电极反应式为___________,电池总反应式为__________。
(3)实验4中的Al作正极还是负极?____________________,原因是____________________。
(4)解释实验5中电流计指针偏向Al的原因:__________________。
(5)根据实验结果,总结在原电池中金属铝作正极还是负极受到哪些因素的影响?____________________。
参考答案:(11分,除注明外,每空1分)(1)不相同
(2)负;Al-3e-===Al3+; 2Al+6H+===2Al3++3H2↑
(3)负极;因为铝能与氢氧化钠溶液反应而镁不能
(4)因为铝被浓硝酸钝化,锌与浓硝酸发生氧化还原反应(2分)
(5)电解质溶液、铝的性质、另一电极材料的活动性强弱 (3分,每答对一个得1分)
本题解析:活泼金属做负极,故实验1中的Al作正极、2中的Al作负极。
(2)在实验3中,Al作负极,电极反应式为Al-3e-===Al3+,电池总反应式为2Al+6H+===2Al3++3H2↑。
(3)实验4中电流表的指针偏向Mg,故Al作负极,因为铝能与氢氧化钠溶液反应而镁不能。
(4)解释实验5中电流计指针偏向Al的原因:因为铝被浓硝酸钝化,锌与浓硝酸发生氧化还原反应。
(5)根据实验结果,总结在原电池中金属铝作正极还是负极受到影响的因素有电解质溶液、铝的性质、另一电极材料的活动性强弱。
本题难度:一般
4、选择题 具有相同电子层数的A、B、C三种元素,已知它们最高氧化物水化物的酸性强弱的顺序是:HAO4>H2BO4>H3CO4,则下列的判断正确的是
A.原子半径A>B>C
B.单质的非金属性A>B>C
C.气态氢化物的稳定性A<B<C
D.阴离子的还原性A>B>C
参考答案:B
本题解析:在元素周期表中,位置自左向右为C、B、A.原子半径C最大,非金属性A最大,氢化物稳定性A最大,阴离子还原性C最大.
本题难度:一般
5、选择题 某元素X的气态氢化物的化学式为H2X,下列叙述正确的是
A.X原子最外层电子层上有6个电子
B.该元素最高价氧化物对应水化物的化学式为HXO3
C.X的单质在常温下一定呈固态
D.X元素的非金属性比氧元素的非金属性强
参考答案:A
本题解析:ⅥA族元素能形成H2X,其最高价氧化物的水化物应为H2XO4,ⅥA元素的氧元素的单质在常温下是气体.
本题难度:一般