| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学必考知识点《氯及其化合物》练习题(十)
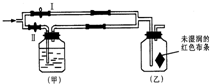 参考答案:C 本题解析: 本题难度:简单 3、选择题 潮湿的Cl2,新制的氯水,次氯酸能使有色布条褪色,其原因是这些物质中含有(?) 参考答案:D 本题解析:氯气没有漂白性,真正起漂白作用的是次氯酸,所以答案选D。 本题难度:简单 4、简答题 氯气在295K、100Kpa时,在1L水中可溶解0.09mol,实验测得溶于水的Cl2约有三分之一与水反应.请回答下列问题: 参考答案:(1)氯气与水反应生成盐酸和次氯酸,反应的离子方程式为:Cl2+H2O?H++Cl-+HClO,故答案为:Cl2+H2O?H++Cl-+HClO; 本题解析: 本题难度:一般 5、选择题 将新制氯水分别滴加到AgNO3溶液、加有酚酞的NaOH溶液、石蕊溶液、品红溶液和Na2CO3溶液中至过量,依次观察到的现象描述合理的一组是( ) 参考答案:新制氯水滴加到AgNO3溶液溶液中新制氯水,发生反应,Ag++Cl-=AgCl↓出现白色沉淀; 本题解析: 本题难度:简单 |
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高中化学必备知识点《元素周期律.. | |