1��ѡ���� ����˵����ȷ����
A��MnO2+4HCl MnCl2 +Cl2 + 2H2O�У��������ͻ�ԭ�����ʵ���֮��Ϊ1:4
MnCl2 +Cl2 + 2H2O�У��������ͻ�ԭ�����ʵ���֮��Ϊ1:4
B��2H2S+ SO2 =3S+2H2O�У���������ͻ�ԭ�������ʵ���֮��Ϊ1:1
C��3S+ 6KOH =2K2S+ K2SO3+3H2O�У��������ͱ���ԭ����Ԫ�����ʵ���֮��Ϊ2:1
D��5NH4NO3=4N2+2HNO3+9H2O�У���Ӧ�з���������Ӧ�ͷ�����ԭ��Ӧ�ĵ�Ԫ�����ʵ���֮��Ϊ5:3
�ο��𰸣�D
�����������
�����Ѷȣ�һ��
2������� д�������л���Ӧ�Ļ�ѧ����ʽ
��1��ʵ������ȡ��Ȳ��______��
��2��2-�������NaOH�Ĵ���Һ�ķ�Ӧ��______��
��3��������Һ��ͨ��������CO2��______��
��4���ɼױ���ȡTNT��______��
��5�����״��Ĵ�������______��
�ο��𰸣���1��̼���ƺ�ˮ��Ӧ��ȡ��Ȳ����ѧ��ӦΪCaC2+2H2O��Ca��OH��2+CH��CH����
�ʴ�Ϊ��CaC2+2H2O��Ca��OH��2+CH��CH����
��2��2-�������NaOH�Ĵ���Һ������ȥ��Ӧ���ɱ�ϩ���Ȼ��ƣ���ѧ��ӦΪCH3CHBrCH3+NaOH��
���������
�����Ѷȣ�һ��
3������� д���йص�Ԫ�ط��Ż�����
��1��ijԪ�������������Ǵ�����������2������Ԫ�ط�����?��
��2��ijԪ��K����M���������ͬ����Ԫ��������?��
�ο��𰸣���1�� C?��2��þ
�����������
�����Ѷȣ�һ��
4������� ��12�֣���˫���ŷ�������з�Ӧ�е���ת�Ƶķ������Ŀ:
2Al+ 6HCl ="=2" AlCl3 + 3 H2��
�˷�Ӧ�У���ԭ����?��?��������?��
?Ԫ�ر�������
�ɴ˿�֪��������ԭ��Ӧ��ʵ����?
�������������дһ��������������ԭ��Ӧ�Ļ�ѧ����ʽ��
? ?
?
�ο��𰸣���12�֣�
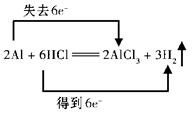
��2�֣�������ʧȥ�͵õ��IJ��÷֣�Al��2�֣���? HCl��2�֣�? Al��2�֣�
��Ӧ�������е���ת�ƣ���ʧ��ƫ�ƣ���2�֣�
CuO+H2D?Cu+H2O��2�֣�������дһ��������ԭ��Ӧ����ʽֻҪ��ȷ�Ϳ��Ե÷֣�
�����������
�����Ѷȣ���
5������� ��һ��������Na2CO3��NaHCO3��������������أ����ų�������ͨ��������Ca��OH��2������Һ�У���ַ�Ӧ��õ��ij�����������1.0g�����Ⱥ�ʣ��Ĺ���������������ϡ���ᷴӦ���ռ���2.2g���壬����ԭ����������Na2CO3��NaHCO3�����������𰸱�����С�����һλ����
�ο��𰸣���NaHCO3����Ϊx��Na2CO3����Ϊy���������
2NaHCO3?��?.?Na2CO3+H2O+CO2��
?168?106?44
?x?106x168?44x168
CO2+Ca��OH��2�TCaCO3��+H2O
44? 100
44x168?1.0g
Na2CO3+2HCl�T2NaCl+H2O+CO2��
106?44
y+106x168? 2.2?g
���x=1.68g��y=4.24g��
��ԭ����������Na2CO3������Ϊ4.24g��NaHCO3������Ϊ1.68g��
���������
�����Ѷȣ�һ��