1、选择题 白磷和红磷可以相互转化,它们在氧气中燃烧后都生成五氧化二磷,这一事实说明了白磷和红磷互为
A.同一单质
B.同位素
C.同素异形体
D.同分异构体
参考答案:C
本题解析:生成同种物质说明含有相同的元素,白磷和红磷是不同的单质而不是核素,所以为同素异形体,C正确。
本题难度:简单
2、实验题 二氧化氯(ClO2)是一种黄绿色有刺激性气味的气体,其熔点为-59℃,沸点为11.0℃,易溶于水。工业上用潮湿的KClO3和草酸(H2C2O4)在60时反应制得。某学生拟有左下图所示的装置模拟制取并收集ClO2。
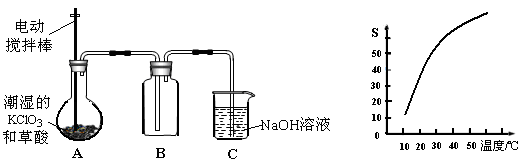
(1)A中反应产物有K2CO3、ClO2和CO2等,请写出该反应的化学方程式:?。
(2)A必须添加温度控制装置,除酒精灯外,还需要的玻璃仪器有烧杯、?;B也必须添加温度控制装置,应该是?(选填“冰水浴”或“热水浴”)装置。
(3)反应后在装置C中可得NaClO2溶液。已知NaClO2饱和溶液中在温度低于38℃时析出晶体是NaClO2・3H2O,在温度高于38℃时析出晶体是NaClO2。根据右上图所示的NaClO2的溶解度曲线,请补充从NaClO2溶液中制得NaClO2的操作步骤:
①?;②?;③洗涤;④干燥。
(4)NaClO2变质可分解为NaClO3和NaCl。取等质量变质前后的NaClO2试样均配成溶液,分别与足量FeSO4溶液反应时,消耗Fe2+的物质的量相同,从电子守恒的角度解释其原因是?。
ClO2很不稳定,需随用随制,产物用水吸收得到ClO2溶液。为测定所得溶液中ClO2的含量,进行了下列实验:
步骤1:准确量取ClO2溶液10.00 mL,稀释成100.00 mL试样;量取V1 mL试样加入到锥形瓶中;
步骤2:调节试样的pH≤2.0,加入足量的KI晶体,静置片刻;
步骤3:加入淀粉指示剂,用c mol・L―1 Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液V2 mL。(已知2 Na2S2O3 + I2 →Na2S4O6 + 2NaI)
(5)判断滴定终点的现象?。原ClO2溶液的浓度为?g / L(用步骤中的字母代数式表示)。
参考答案:(1)2KClO3+ H2C2O4 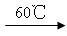 ?K2CO3+CO2↑+2ClO2↑+H2O ?(2分)
?K2CO3+CO2↑+2ClO2↑+H2O ?(2分)
(2)温度计 冰水浴 (2分)
(3)蒸发结晶 趁热过滤 (2分)
(4)根据氧化还原反应过程中电子转移守恒,反应整个过程中氯元素最终为-1价,所以FeSO4所失去的电子数相等,消耗的FeSO4的量也相等。 (2分)
(5)加到最后一滴时,溶液的颜色突然由蓝色变为无色,且半分钟不变化(2分) 135cV2/V1(2分)
本题解析:(1)A中反应产物有K2CO3、ClO2和CO2等,加热60℃,氯酸钾和草酸反应生成碳酸钾、二氧化碳、二氧化氯和水,反应方程式为:2KClO3+H2C2O4=K2CO3+CO2↑+2ClO2↑+H2O;
(2)要控制温度必须使用温度计测量温度,在60℃时反应制得,应用水浴加热,可用烧杯(或水浴锅),二氧化氯的熔点较低,为收集二氧化氯,应在较低温度下进行,所以应该采用冰水浴,故答案为:冰水浴;?烧杯(或水浴锅),温度计;
(3)根据信息NaClO2饱和溶液中在温度低于38℃时析出晶体是NaClO2・3H2O,在温度高于38℃时析出晶体是NaClO2。根据右上图所示的NaClO2的溶解度曲线,随着温度升高溶解度增大,因此请补充从NaClO2溶液中制得NaClO2的操作步骤为蒸发结晶和趁热过滤。
(4)根据氧化还原反应过程中电子转移守恒,反应整个过程中氯元素最终为-1价,所以FeSO4所失去的电子数相等,消耗的FeSO4的量也相等。
(5)判断滴定终点的现象为滴定终点时,I2完全反应,溶液由蓝色变为无色,故答案为:蓝色变为无色且半分钟不变化;
(6)设原ClO2溶液的浓度为x,
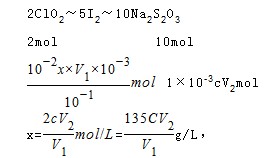
本题难度:一般
3、选择题 在探究新制饱和氯水成分的实验中,下列根据实验现象得出的结论不正确的是
A.氯水的颜色呈浅绿色,说明氯水中含有Cl2
B.向氯水中滴加硝酸酸化的AgNO3溶液,产生白色沉淀,说明氯水中含有Cl-
C.向氯水中加入NaHCO3粉末,有气泡产生,说明氯水中含有H+
D.向FeCl2溶液中滴加氯水,溶液颜色变成棕黄色,说明氯水中含有HClO
参考答案:D
本题解析:A、氯气是黄绿色气体,因此氯水的颜色呈浅绿色,说明氯水中含有Cl2,A正确;B、向氯水中滴加硝酸酸化的AgNO3溶液,产生白色沉淀,白色沉淀是氯化银,这说明氯水中含有Cl-,B正确;C、向氯水中加入NaHCO3粉末,有气泡产生,气体是CO2,这说明氯水中含有H+,C正确;D、向FeCl2溶液中滴加氯水,溶液颜色变成棕黄色,说明反应中有氯化铁生成。由于氯气也能把氯化亚铁氧化生成氯化铁,因此不能说明氯水中含有HClO,D不正确,答案选D。
本题难度:一般
4、选择题 如图装置,将溶液A逐滴加入固体B中,下列叙述正确的是( )
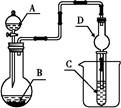
A.若A为浓盐酸,B为MnO2,C中盛品红溶液,则C中溶液褪色
B.若A为醋酸,B为贝壳,C中盛CaCl2溶液,则C中溶液变浑浊
C.若A为浓硝酸,B为铜,C中盛KI 淀粉溶液,则C中溶液变蓝
淀粉溶液,则C中溶液变蓝
D.若A为浓硫酸,B为Na2SO3固体,C中盛石蕊试液,则C中溶液先变红后褪色
参考答案:C
本题解析:A项不加热,不产生氯气,A项错误;B项将CO2通入CaCl2溶液中,两者不反应,不会产生沉淀,B项错误;Cu与浓HNO3反应放出NO2气体,NO2有氧化性,通入KI淀粉溶液中能生成I2,遇淀粉变蓝色,C项正确;SO2为酸性气体,只能使石蕊变红,不能漂白石蕊,D项错误。
本题难度:一般
5、简答题 (1)用滴管将新制的饱和氯水逐滴滴入含酚酞的氢氧化钠的稀溶液中,当滴到最后一滴时,红色突然褪去.产生该现象的原因可能有两个:
①是由于______;②是由于______.?
用实验证明红色褪去的原因是①或者是②,其方法是:____________.
(2)在一定条件下氯气可与氯化铵发生反应:xCl2+yNH4Cl→yNCln+(x+y)HCl,当消耗6.72L标准状况下的氯气时,生成0.10mol氮的氯化物,则此氮的氯化物的化学式为______.
参考答案:(1)因酚酞遇碱变红,将新制氯水慢慢滴入含酚酞的NaOH稀溶液中,当滴到最后一滴时红色突然褪去,则可能为氯水中的酸性与碱反应,使NaOH减少,而能使溶液由红色变成无色;
也可能为氯水中的次氯酸有漂白性,使溶液由红色变成无色.
因次氯酸漂白后的溶液再加NaOH溶液不会恢复颜色,向褪色溶液中再滴加NaOH溶液,若红色再现,则是①;若红色不再现,则是②.
故答案为:氯水中H+与碱中和;氯水中HClO强氧化性所致;向褪色溶液中再滴加NaOH溶液,若红色再现,则是①;若红色不再现,则是②;
(2)xCl2+yNH4Cl→yNCln+(x+y)HCl,根据氧化还原反应中得失电子数相等配平该方程式,
(n+3)Cl2+2NH4Cl=2NCln+8HCl
? n+3?2?
?6.72L22.4L/mol 0.10mol
所以n=3,该氯化物的化学式为NCl3.
故答案为:NCl3.
本题解析:
本题难度:一般