1��ѡ���� �������±�ص�������ȷ����
A��±������(X��)ֻ�л�ԭ�Զ���������
B��ijԪ���ɻ���̬�������̬����Ԫ��һ��������
C��ʧ�����ѵ�ԭ�ӻ�õ��ӵ�����һ��ǿ
D��±�����������ķ���ʽ��ΪX2O7
�ο��𰸣�A
�����������
�����Ѷȣ�һ��
2��ѡ���� ����������ͨ���С��������֮˵�������ᡱָ���ᡢ��������ᣬ�����ָ�ռ�ʹ��
��1�������ʷ���ĽǶȷ���������˵���в�ǡ����һ��������__________�����ѧʽ����
��2���������м���ŨH2SO4ʱ�����а������ɡ��������������ڵ��²����������ԭ�����__________������ţ���
A��ŨH2SO4������ˮ��
B��������лӷ���
C���������ʵ��ܽ�����¶����߶�����
��3�������ᡱ�������ܽ�����ͽ���������
�����п�״�����ڳ������ܹ�ȫ������������Ũ�������______������ţ���
A��Au? B��Ag? C��Al? D��Fe
�ڽ���ͭͶ��ϡ�����в�������Ӧ�����ټ���H2O2��Һ��ͭ��ʼ�ܽ⣬��Һ��Ϊ��ɫ��д���÷�Ӧ�����ӷ���ʽ__________________________��
��4���ռ������Һ��������CO2���塣����0��1molNaOH����Һ����һ����CO2����Һ����С�����ɣ��Ƶù�������Ϊ8g�������ù�����____________���ѧʽ����
�ο��𰸣���1��Na2CO3��1�֣�
��2��A��2�֣�
��3����B��2�֣���Cu+H2O2+2H+=2H2O��2�֣�
��4��NaHCO3��Na2CO3��2�֣�
�����������1��Na2CO3�����Σ����Բ�ǡ����
��2��Ũ���������ˮ�ԣ�����Ũ�����е�ˮ���ٽ�HCl�Ļӷ�������ˮ���أ���ѡA�
��3��H2O2���������ԣ���H+����ʱ��Cu������Cu+H2O2+2H+=2H2O
��4����CO2��NaOHȫ������Na2CO3������Ϊ5��3g����ȫ������NaHCO3������Ϊ8��4g��ʵ�ʹ�����������Ϊ8g�����Է�Ӧ������Na2CO3��NaHCO3�Ļ���
�����Ѷȣ�һ��
3��ѡ���� ����������ɫ����ԭ���Ƿ���ͬ����ʶ�У���ȷ��һ���ǣ�������
�ٶ�������ʹƷ����Һ��ɫ?�ڻ���̿ʹ��īˮ��ɫ?����ˮʹ��ɫ������ɫ��
A���ٺ͢�ԭ����ͬ
B���ٺ͢�ԭ����ͬ
C���ں͢�ԭ����ͬ
D���٢ڢ�ԭ��������ͬ
�ο��𰸣�����ѡ������ɫԭ���ֱ�Ϊ���ٶ����������Ư���ԣ���ˮ���ɵ��������Ʒ����Ϊ��ɫ���ʣ�
�ڻ���̿������������ʹ��īˮ��ɫ��
����ˮ�еĴ��������ǿ�����ԣ������л�ɫ��Ϊ��ɫ���ʣ�
���Ԣ٢ڢ۵���ɫԭ��������ͬ��
��ѡD��
���������
�����Ѷȣ�һ��
4������� ��������(NaC1O2)��һ����Ҫ�ĺ�������������Ҫ����ˮ�������Լ�ɰ�ǣ���֬��Ư����ɱ���������ǹ������ⷨ�����������ƵĹ�������ͼ��
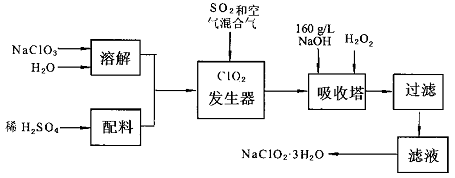
��֪����NaC1O2���ܽ�����¶����߶������ʵ������¿ɽᾧ����NaC1O2��3H2O��
�ڴ�C1O2�ֽⱬը��һ����ϡ����������ϡ�͵�10%���°�ȫ��
I��������������̻ش���������
��1���������й�����������ÿ�����?
��2���������ڵķ�Ӧ�Ļ�ѧ����ʽΪ?�����������¶Ȳ��ܳ���20�棬��Ŀ����?��
��3���ڼ�����Һ��NaC1O2�Ƚ��ȶ���������������Ӧά��NaOH�Թ������ж�NaOH�Ƿ�����ļ�ʵ�鷽����?��
��4������Һ�еõ�NaC1O2��3H2O�־����ʵ�����������?��
II�����������е�ԭ��NaC1O3��������ͨ���ȵ��ռ���Һ���ؽᾧ�͵õ��Ƚϴ����IJ�Ʒ������ͨ�����������ȼ���Ʊ���
��1���ȼҵ�е�ԭ��Ϊ?��ԭ����Ҫ������ԭ����?��������ƷΪ?
��2����ҵ����NaC1O3�Ļ�ѧ����ʽΪ?
�ο��𰸣���1��ϡ��C1O2�Է�ֹ��ը����2��2NaOH+2C1O2+H2O2=2NaC1O2+2H2O+O2?��ֹH2O2�ֽ�
��3�������ⶨ����������Һ��pH��?��4����������ȴ�ᾧ������
��1������ʳ��ˮ?��ֹ�������ӽ���Ĥ?����?��2��3Cl2+6NaOH==5NaCl+NaClO3+3H2O
�����������1��������Ӧ������C1O2���ȶ��ֽⱬը��������������ð���ϡ����0%���°�ȫ��������2���������ڵķ�Ӧ�Ļ�ѧ����ʽΪ��2NaOH+2C1O2+H2O2=2NaC1O2+2H2O+O2���������ⲻ�ȶ����������ֽ⡣���������¶Ȳ��ܳ���20�棬��Ŀ���Ƿ�ֹH2O2�ֽ⡣��3���ж�NaOH�Ƿ�����ļ�ʵ�鷽���Dzⶨ����������Һ��pH����4������Һ�еõ�NaC1O2��3H2O�־����ʵ������������Ƚ���Һ����ˮ�ֵõ�NaC1O2�ı�����Һ���ٽ����¶ȣ����������ܽ�����¶ȵ����߶��������¶ȵĽ��Ͷ���С���ص㣬��ȴ�ᾧ�������˼���NaC1O2��3H2O��II����1���ȼҵ�е�ԭ��Ϊ����ʳ��ˮԭ����Ҫ��������Ϊ�������������ӽ���Ĥ��������Ʒ��������������Ʒ���������������ơ���2����ҵ����NaC1O3�Ļ�ѧ����ʽΪ3Cl2+6NaOH==5NaCl+NaClO3+3H2O?��2)���Ʒ����ȼҵ��ԭ������Ʒ��֪ʶ��
�����Ѷȣ�����
5��ʵ���� ��10�֣���ͼ��ʵ������ȡ���ռ�Cl2��װ�á�A��Cl2����װ�ã���E��Ӳ�ʲ�������װ��ϸ��˿����FΪ����Ĺ��ƿ���ձ�GΪβ������װ�á�
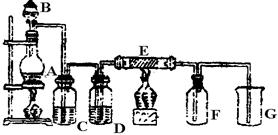
�Իش�
��1��A�з����Ļ�ѧ��Ӧ����ʽΪ?��
��2��C��D��G�и�װ��ҩƷ��C__________��D__________��G__________��
��3��E�е�����Ϊ?����Ӧ����ʽΪ?��
��4��д��G�з�Ӧ�����ӷ���ʽ?��
��5������Cl2��SO2�����ʵ������Ư�����ü������û�ѧ����ʽ����ԭ��?��
�ο��𰸣���1��MnO2+4HCl��Ũ�� MnCl2+Cl2��+2H2O
MnCl2+Cl2��+2H2O
��2������Na Cl��Һ��Ũ H2SO4?��NaOH��Һ
��3�����ҷ�Ӧ�������غ�ɫ���غ�ɫ�����̣��ų������ȣ�2 Fe +3 Cl2�T�T2FeCl3 ����
���ԣ�
��4��Cl2+2 OH���T�TCl��+ ClO��+H2O?(2��)
��5��Cl2+SO 2+2H2O �T�TH2SO4+ 2HCl?(2��) �����1��
�����������1��ʵ�����ö���������Ũ�����������ȡ�������ʷ�ӦΪMnO2+4HCl��Ũ�� MnCl2+Cl2��+2H2O��
MnCl2+Cl2��+2H2O��
��2������װ�ÿ�֪C��DΪ��������������װ�ã�������Ϊ��ϻӷ�����HCl���壬���ñ���ʳ��ˮ��ȥHCl���壬�����������������Ũ�����������������ȡҪ���Ⱦ���������Cװ���Լ�Ϊ����ʳ��ˮ��Dװ���Լ�ΪŨ���ᡣ�������������Ӧ���ü�Һ����������Һ������GӦ��װ����������Һ��
��3��E������������������Ӧ�����Ȼ����������ǣ����ҷ�Ӧ�������غ�ɫ���غ�ɫ�����̣��ų������ȣ���Ӧ����ʽΪ2 Fe +3 Cl2 2FeCl3 ��
2FeCl3 ��
��4��G�з�ӦΪ�������������Ʒ�Ӧ�����Ȼ��ơ��������ƺ�ˮ�����ӷ���ʽΪ��
Cl2+2 OH���T�TCl��+ ClO��+H2O
��5��Cl2����ǿ�����Ժ�SO2���л�ԭ�Ե����ʵ�����Ϻ���������ԭ��Ӧ��
Cl2+SO 2+2H2O �T�TH2SO4+ 2HCl
������������������ȡԭ�ϡ�ԭ�����ռ������������β�������ȵȡ�
�����Ѷȣ�һ��