1、选择题 下列变化过程中,没有破坏化学键的是( )
A.氯化钠的融化
B.HCl溶于水
C.酒精溶于水
D.水的通电分解
参考答案:A、氯化钠属于离子晶体,在熔化状态下电离出自由移动的阴阳离子,离子键被破坏,故A错误.
B、HCl溶于水,在水分子的作用下,电离出自由移动的阴阳离子,所以化学键被破坏,故B错误.
C、酒精在水中的扩散,没有发生电离,化学键没有变化,变化的是分子间作用力,故C正确;
D、电解水,水在通电条件下,发生了化学反应,分解生成氢气和氧气,所以化学键被破坏,故D错误.
故选:C
本题解析:
本题难度:简单
2、填空题 (5分)依据事实,写出下列反应的热化学方程式。
(1)在25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为_________________________________________。
(2)盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得,但可通过间接的方法测定。现根据下列3个热化学方程式:
Fe2O3(s)+3CO(g)="=" 2Fe(s)+3CO2(g) △H=- A kJ/mol
3Fe2O3(s)+ CO(g)==2Fe3O4(s)+ CO2(g) △H=- B kJ/mol
Fe3O4(s)+CO(g)==3FeO(s)+CO2(g) △H= + C kJ/mol
写出CO气体还原FeO固体得到Fe固体和CO2气体的热化学方程式:

参考答案:(共5分)
(1)CH3OH(l)+3/2 O2(g)=CO2(g) +2H2O(l) △H="-725.76kJ/mol " (2分)
△H="-725.76kJ/mol " (2分)
(2) CO (g)+ FeO (s)=CO2(g) +Fe (s) 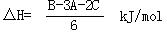 (3分)
(3分)
本题解析:略
本题难度:一般
3、选择题 将铁粉和硫粉混合后加热,待反应一发生即停止加热,反应仍可以继续进行,直至反应完全生成新物质硫化亚铁.该现象说明了
A.该反应是吸热反应
B.该反应是放热反应
C.铁粉和硫粉在常温下可以发生反应
D.生成物硫化亚铁的总能量高于反应物铁粉和硫粉的总能量
参考答案:B
本题解析:加热能够达到反应所需要的条件.反应后停止加热,由于反应自身释放出的能量能够维持该反应所需要的温度条件,所以反应能够进行.从现象上看,该反应是放热反应.
本题难度:简单
4、选择题 CO2的的资源化利用是解决温室效应的重要途径。以下是在一定条件下用NH3捕获CO2生成重要化工产品三聚氰胺的反应:NH3+CO2→ +H2O
+H2O
下列有关三聚氰胺的说法正确的是
A.分子式为C3H6N3O3
B.分子中既含极性键,又含非极性键
C.属于共价化合物
D.生成该物质的上述反应为中和反应
参考答案:C
本题解析:A、分子式为C3H3N3O3,错误;B、该分子中没有非极性键,错误;C、正确;D、该反应不是中和反应,中和反应是酸碱反应。
本题难度:简单
5、选择题 下列判断正确的是( )
A.离子键被破坏的变化一定是化学变化
B.晶体中一定存在化学键
C.含有离子键的化合物一定是离子化合物
D.共价键越强,分子性质越不活泼
参考答案:A、离子化合物在熔融时或着溶解时,离子键都会发生断裂,但没有新的化学键形成,则不是化学变化,故A错误;
B、稀有气体元素形成的都是单原子分子,分子之间只存在分子间作用力,没有化学键,故B错误;
C、离子键只存在于离子化合物中,可能含有共价键,共价化合物只存在共价键,故C正确;
D、有时候某些分子中某个共价键很强,但是化学反应并不发生在这个化学键上而是发生在其他化学键上,则分子性质活泼,可以简单理解成分子活泼是分子整体的性质,而一个分子并非只有一个化学键,故D错误;
故选C.
本题解析:
本题难度:简单