1、填空题 对于在密闭容器中进行的反应2SO2+O2

2SO3,其他条件不变,只改变一个反应条件,将生成SO3的反应速率的变化填入由表中空格里.(选填增大、减小或不变)
| ? | 改变条件 | 速率变化
①
降低温度
?
②
增加O2浓度
?
③
使用V2O5做催化剂
?
④
压缩气体
?
参考答案:①温度对化学反应速率的影响是:温度越高,反应速率越大,温度越低,反应速率越小,故答案为:减小.
①浓度对化学反应速率的影响是:浓度越大,反应速率越大,浓度越小,反应速率越小,故答案为:增大.
③催化剂对化学反应速率的影响是:加入正催化剂,反应速率加快,V2O5是其正催化剂,所以反应速率加快,故答案为:增大.
③压强对化学反应速率的影响是:增大压强,反应速率加快,减小压强,反应速率减慢,压缩体积,增大体系压强,故答案为:增大.
本题解析:
本题难度:简单
2、选择题 一定量的盐酸和过量的铁粉反应时,为了增大反应速率,且不影响生成氢气的总量,可向盐酸中加入适量的
A.NaOH(s)
B.NaCl(s)
C.CuSO4 (s)
D.H2O
参考答案:C
本题解析:略
本题难度:一般
3、填空题 如下图所示,把试管放入盛有25℃时饱和石灰水的烧杯中,试管中开始放入几小块镁片,再滴入5mL盐酸,试回答下列问题。
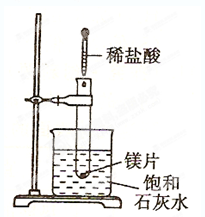
⑴实验中观察到的现象是________ ____________ _______________
_____________________ ______ _________。
⑵产生上述现象的原因是____ _______ ______________
_____________________ _____ _________。
⑶写出有关反应的离子方程式_ _______________________。
⑷由实验推知,MgCl2溶液和H2的总能量____________(填“大于”、“小于”或“等于”)镁片和盐酸的总能量。
参考答案:(1)①镁片上有大量气泡产生;②镁片逐渐溶解;③烧杯中溶液变浑浊
(2)镁与盐酸反应产生氢气,该反应为放热反应,Ca(OH)2在水中溶解度水温度升高而减小,故析出Ca(OH)2固体
(3)Mg+2H+=Mg2++H2 ↑ (4)小于
本题解析:镁是活泼的金属,能和盐酸反应生成氢气和氯化镁。该反应是放热反应,说明反应物的总能量高于生成物的总能量。溶液温度升高,但由于Ca(OH)2在水中溶解度水温度升高而减小,所以析出Ca(OH)2固体。
本题难度:一般
4、选择题 在一可变容积的密闭容器中进行反应:C(s) + H2O(g)=" CO(g)" + H2(g),下列条件能使反应速率增大的是
A.增加C的量
B.将容器的体积缩小一半
C.保持体积不变,充入N2,使体系的压强增大
D.保持压强不变,充入N2,使容器的体积变大
|
参考答案:B
本题解析:改变反应速率的因素有内因(决定性因素―反应物本身的性质)、外因(外界因素:如浓度、温度、压强、催化剂、光、超声波、电磁波等);
A错,增加C的量,反应的浓度不变,反应速率不变;
B正确,将容器的体积缩小一半,气体物质的浓度增大,化学反应速率增快;
C错,保持体积不变,充入N2,表面上压强增大,但体系中各组分的浓度不变,化学反应速率不变;
D错,保持压强不变,充入N2,使容器的体积变大,体系中各组分的浓度变小,反应速率减慢;
本题难度:一般
5、填空题 (8分)如图,曲线表示在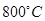 时,和某反应有关的物质A、B、C的物质的量浓度从开始反应至4分钟时的变化图像,试回答:
时,和某反应有关的物质A、B、C的物质的量浓度从开始反应至4分钟时的变化图像,试回答:
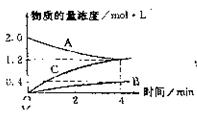
(1)该反的反应物是 。
(2)4分钟时,C的浓度是B的 倍。
(3)该反应的化学方程式是
(4)反应开始至4分钟,若用A的浓度来表示该反应的平均速率为
参考答案:(1)A (2)3 (3)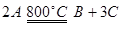 (4)
(4)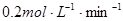
本题解析:(1)根据图像可知,A的浓度是减小的,B、C浓度是增加的,所以A是反应物,B、C是生成物。
(2)4分钟时,C、B的浓度分别是1.2mol/L和0.4mol/L,所以4分钟时,C的浓度是B的3倍。
(3)4min时,A的浓度减少了0.8mol/L,B和C的浓度分别增加了0.4mol/L和1.2mol/L,所以根据反应速率之比是相应的化学计量数之比可知,反应的方程式是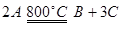
(4)反应速率通常用单位时间内浓度的变化量来表示,所以A的反应速率是0.8mol/L/4min=0.2mol/(L・min)。
本题难度:一般