1、选择题 下列关于实验现象的描述不正确的是( )
A.用锌片做阳极,铁片做阴极,电解氯化锌溶液,铁片表面出现一层锌
B.把铜片和铁片紧靠在一起浸入稀硫酸中,铁片表面出现气泡,铜片表面无气泡
C.把锌粒放入盛有盐酸的试管中,加入几滴氯化铜溶液,气泡放出速率加快
D.把铜片插入三氯化铁溶液中,在铜片表面出现一层铁
参考答案:A.该装置构成电镀池,锌片作镀层,铁片作镀件,电解氯化锌溶液时,在铁片表面镀上一层锌,故A正确;
B.铜、铁和稀硫酸构成原电池,铁作负极,铜作正极,铜电极上氢离子得电子生成氢气,故B错误;
C.锌置换出铜,铜、锌和稀盐酸构成原电池,原电池加快反应速率,故C正确;
D.铜和氯化铁溶液反应生成氯化亚铁、氯化铜,所以不能在铜片表面析出一层铁,故D错误;
故选BD.
本题解析:
本题难度:一般
2、选择题 可逆反应A(g)+3B(g)?2C(g)+2D(g)在不同条件下的反应速率如下,其中反应速率最快的是( )
A.v(A)=0.4mol/(L?s)
B.v(B)=0.6mol/(L?s)
C.v(C)=0.4mol/(L?s)
D.v(D)=0.45mol/(L?s)
参考答案:反应速率除以对应各物质的化学计量数为:
A、0.4mol/(L?S)1=0.4mol/(L?s)
B、0.6mol/(L?s)3=0.2mol/(L?s)
C、0.40.4mol/(L?s)2=0.2mol/(L?s)
D、0.45mol/(L?s)2=0.225mol/(L?s)
反应快慢的顺序为:A>D>B=C,所以A最快.
故选A
本题解析:
本题难度:一般
3、选择题 在相同温度下,将H2和N2两种气体按不同比例通入相同的恒容密闭容器中,发生反应:3H2+N2 2NH3。
2NH3。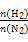 表示起始时H2和N2的物质的量之比,且起始时H2和N2的物质的量之和相等。下列图像正确的是(?)
表示起始时H2和N2的物质的量之比,且起始时H2和N2的物质的量之和相等。下列图像正确的是(?)
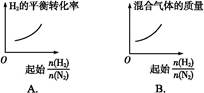
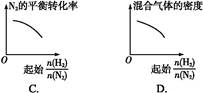
参考答案:D
本题解析:A中,随着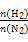 的增大,氢气含量增多,氢气的平衡转化率降低,A错误;随着
的增大,氢气含量增多,氢气的平衡转化率降低,A错误;随着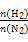 的增大,氢气含量增多,混合气体的质量减小,B错误;随着
的增大,氢气含量增多,混合气体的质量减小,B错误;随着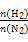 的增大,氢气含量增多,氮气的平衡转化率增大,C错误;随着
的增大,氢气含量增多,氮气的平衡转化率增大,C错误;随着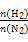 的增大,氢气含量增多,混合气体的质量减小,容器体积不变,则混合气体的密度减小,D正确。
的增大,氢气含量增多,混合气体的质量减小,容器体积不变,则混合气体的密度减小,D正确。
本题难度:一般
4、选择题 反应2A+3B=C+2D在2L的密闭容器中进行,半分钟后,C的物质的量增加了0.3 mol,则此反应的平均速率表达正确的是
A.v(C)=0.01 mol・L-1・s-1
B.v(B)=0.03 mol・L-1・s-1
C.v(A)=0.01 mol・L-1・s-1
D.v(D)=0.02 mol・L-1・s-1
参考答案:C
本题解析:考查化学反应速率的概念和有关计算。半分钟内C的物质的量增加了0.3mol,所以用C物质表示的反应速率是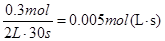 ,又因为速率之比是相应的化学计量数之比,答案选C。
,又因为速率之比是相应的化学计量数之比,答案选C。
考点:化学反应速率
本题难度:一般
5、选择题 下列说法不正确的是? ( )
①0.1 mol・L-1盐酸和0.1 mol・L-1醋酸分别与0.2 mol・L-1氢氧化钠溶液反应的速率相同
②0.1 mol・L-1盐酸和0.1 mol・L-1硝酸分别与大小相同的大理石反应的速率不同
③大理石块与大理石粉末分别与0.1 mol・L-1盐酸反应的速率不同
④已知t℃时反应N2(g)+3H2(g) 2NH3(g) ΔH<0的速度为v,若降低温度,正反应速率加大
2NH3(g) ΔH<0的速度为v,若降低温度,正反应速率加大
⑤合成氨中及时分离出氨气后可减小反应速率
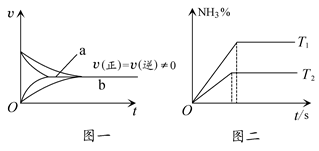
⑥在合成氨反应中,相同条件下在有催化剂时(a)和无催化剂时(b)速率时间图像可用下图一表示
⑦在合成氨反应中,不同温度下(T2>T1)的NH3的体积分数与时间的关系图像可用图二表示
A.除①⑦外
B.除③⑤⑥外
C.除③⑤外
D.除③⑥⑦外
参考答案:C
本题解析:0.1 mol・L-1的醋酸c(H+)小,反应速率小,①不正确,0.1 mol・L-1的盐酸和硝酸c(H+)相同,反应速率相同,②不正确,大理石块与大理石粉表面积不同,反应速率不同,③正确。降低温度,反应速率减小,④不正确,合成氨分离出氨时平衡正向移动,反应混合物浓度减小,⑤正确。使用催化剂,反应速率加快,平衡速率不相等,⑥不正确,温度低时,反应速率慢,转化率随时间变化应小于温度高时,⑦不正确。
本题难度:一般