1、填空题 由原子序数依次增大的五种短周期元素A、B、C、D、E,已知A、E同主族,A元素的原子半径最小,B元素原子的最外层电子数是内层电子数的2倍,C元素最高价氧化物的水化物与其氢化物反应生成一种盐;A、B、C、E四种元素分别都能与D元素形成原子个数比不相同的多种常见化合物,回答下列问题:
(1)B在周期表中的位置是?,C元素的单质的电子式?。
(2)写出同时含A、B、C、D四种元素的一种盐的化学式?。
(3)E与D形成的一种化合物与BD2发生氧化还原反应,该反应的化学方程式为。
(4)用A和D两元素组成的单质可以制成一种燃料电池,电池中装有浓KOH溶液。用多孔的惰性电极浸入浓KOH溶液中,两极均有特制的防止气体透过的隔膜,在一极通入A的单质,另一极通入D的单质。则该电池正极的电极反应式为?。
(5)化合物C2A4和C2D4的液体曾被用作火箭推进剂,燃烧反应的生成物是一种气态单质和一种化合物,它们对环境无污染。已知1mol C2A4和C2D4完全反应生成两种气体时放出热量516.8KJ,则该反应的热化学方程式为?。
参考答案:(1)第二周期IVA族(2分);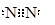 (2分);
(2分);
(2)NH4HCO3或(NH4)2CO3(2分)
(3)2Na2O2+2CO2=2Na2CO3+O2(2分)(4)O2+2H2O+4e-=4OH-(2分)
(5)2N2H4(l)+N2O4(l)=3N2(g)+4H2O(g)?H=-1033.6KJ・mol-1(2分)
本题解析:
试题分析;据题意可知A为氢原子、B为碳、 C为氮 D为氧。碳是元素周期表中的第六号元素。周期系数等于电子层数,在主族中,族系数等于最外层电子数,故(1)B的位置为第二周期IVA族。氮气有三对共用电子对,所以它的电子式为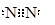 (2)据题意可知该盐为NH4HCO3或(NH4)2CO3
(2)据题意可知该盐为NH4HCO3或(NH4)2CO3
考点;考查元素周期表的相关知识以及原电池的相关知识
本题难度:一般
2、填空题 (11分)几种短周期元素的原子半径及主要化合价见下表:

分析上表的有关数据,并结合已学过知识,请用化学用语到答下列问题。
(1)写出D元素在周期表中的位置___________________。
(2)含20克F的最高价氧化物的水化物的稀溶液与足量B的氢化物的稀溶液反应放出热量a kJ,请写出该反应的热化学反应方程式____________________________。
(3)用电子式表示F2C2的形成过程______________________________。
(4)BA2能与盐酸反应得到黄绿色气体,试写出化学反应方程式:__________________,
B、C、F的最高价氧化物对应的水化物形成溶液,浓度均为0.1mol/L时,pH由大到小的顺序为___________________。
(5)lmol F2A2与水反应生成的溶液与lL 0.5mol/LEB3溶液反应的离子方程式为
______________________________。
参考答案:(1)第三周期ⅣA族(1分)
(2) HCl(aq)? +? NaOH(aq) =H2O(l)? +? NaCl(aq);△H=-2akJ/mol(2分)
(3)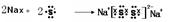 (2分)
(2分)
(4)8HC1 + 2C1O2===5C12↑ + 4H2O(2分),? NaOH>HClO4>H2SO4(2分)
(5)Al3++4OH- = [Al(OH)4]-(写为A1O2-也可) (2分)
本题解析:本题考查元素推断及元素周期表和周期律的有关知识。由表中数据结合元素周期表。可以确定A、B、C、D、E、F分别为O、Cl、S、Si、Al、Na。(1)Si处于元素周期表中第三周期ⅣA族;(2)20克NaOH和HCl反应放出热量a kJ,则1molNaOH和HCl反应放出热量就是2a kJ,则反应的热化学反应方程式为HCl(aq) +NaOH(aq)=H2O(l)+NaCl(aq);△H=-2akJ/mol。(3)Na2S2可以类比于Na2O2,再写Na2S2形成过程可表示为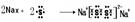 。(4)ClO2与盐酸反应得到黄绿色气体――Cl2,根据电子得失守恒可写出反应的方程式为8HC1+2C1O2=5C12↑+4H2O。HClO4、H2SO4、NaOH中前两者为强酸,后者是强碱,pH分别为1、0.7、11,pH由大到小的顺序为NaOH>HClO4>H2SO4。(5)lmolNa2O2与水反应可生成2molNaOH,lL 0.5mol/L AlCl3中AlCl3的物质的量为0.5mol,2molNaOH恰好能将Al3+转化为A1O2-,故反应的离子方程式为Al3++4OH- = A1O2-+2H2O。
。(4)ClO2与盐酸反应得到黄绿色气体――Cl2,根据电子得失守恒可写出反应的方程式为8HC1+2C1O2=5C12↑+4H2O。HClO4、H2SO4、NaOH中前两者为强酸,后者是强碱,pH分别为1、0.7、11,pH由大到小的顺序为NaOH>HClO4>H2SO4。(5)lmolNa2O2与水反应可生成2molNaOH,lL 0.5mol/L AlCl3中AlCl3的物质的量为0.5mol,2molNaOH恰好能将Al3+转化为A1O2-,故反应的离子方程式为Al3++4OH- = A1O2-+2H2O。
本题难度:一般
3、选择题 下列各组微粒具有相同质子数和电子数的是?(?)
A.H3O+、NH4+、Na+、HF
B.OH-、F-、O2-、Ne
C.CH4、NH3、H2O、HF
D.O2-、F-、Mg2+、Al3+
参考答案:C
本题解析:略
本题难度:简单
4、选择题 从下列事实所得出的相应结论正确的是?(?)
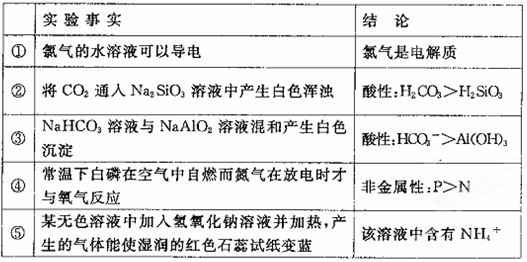
A.②③⑤
B.③④⑤
C.①②③
D.全部
参考答案:A
本题解析:①氯气为单质,既不是电解质也不是非电解质;导电是因为其反应生成HCl和HClO;
②强酸制弱酸,正确;
③强酸制弱酸,正确;
④这个要考虑结构,氮气中氮氮三键,具有很高的键能,故温度,非金属性N>P
⑤中学只有氨气为碱性气体,正确
本题难度:一般
5、选择题 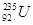 ?是重要的核工业原料,但在自然界的丰度很低,
?是重要的核工业原料,但在自然界的丰度很低,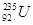 的浓缩一直为国际社会关注。下列有关:
的浓缩一直为国际社会关注。下列有关: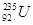 说法正确的是
说法正确的是
A.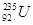 与
与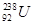 ?互为同位素
?互为同位素
B.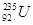 原子核外有143个电子
原子核外有143个电子
C: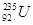 与
与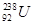 是同一种核素
是同一种核素
D. 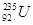 原子核中含有92个中子
原子核中含有92个中子
参考答案:A
本题解析:A、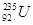 与
与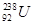 23892U质子数相同,中子数不同,互为同位素,正确;B、
23892U质子数相同,中子数不同,互为同位素,正确;B、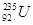 原子核外有92个电子,错误;C、
原子核外有92个电子,错误;C、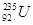 与
与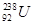 质子数相同,中子数不同,是2种核素,错误;D、
质子数相同,中子数不同,是2种核素,错误;D、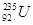 原子核中含有235-92=143个中子,错误,答案选A。
原子核中含有235-92=143个中子,错误,答案选A。
本题难度:一般