1������� (10��)A��B��C��D��E��F����������һ��������������ͼ��ʾ���ת����ϵ�����з�Ӧ�����������Ѹ�����
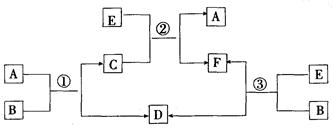
(1)����Ӧ�١��ڡ��۾�Ϊˮ��Һ�е��û���Ӧ��A��D��EΪ±�ص��ʣ���A��D��E����������ǿ������˳��Ϊ?������A�Ļ�ѧʽ��?��
(2)��B��ˮ��C��һ���д��ԵĻ����E��һ����ɫ����ζ���ж����壬��Ӧ�ٵĻ�ѧ����ʽ��?
(3)��BΪһ�ֵ���ɫ���壬��ɫֲ��Ĺ�����úͺ������ÿ�ʵ����Ȼ����D��E��ѭ������Ӧ�ٵ����ӷ���ʽ��?���ڷ�Ӧ���У�������1 molD����ת�Ƶ�����ĿΪ?��
�ο��𰸣�(1)EAD? Br2?(2)3Fe+4H2O(g)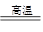 Fe3O4+4H2
Fe3O4+4H2
(3)2Na2O2+2H2O=4Na++4OH-+O2��? 2NA?(ÿ��2�֣���10��)
�������������������ͼ�⣬�ؼ�����ͻ�Ƶ㡣
��1��A��D��EΪ±�ص��ʣ����Ը����û���Ӧ�٢ڢۿ�֪��E��������A���壬D�ǵ��ʵ⡣���A��D��E����������ǿ������˳��ΪEAD��
��2��C��һ���д��ԵĻ������C������������������A������D����������Ӧ�ٵĻ�ѧ����ʽ��3Fe+4H2O(g)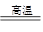 Fe3O4+4H2��
Fe3O4+4H2��
(3)��BΪһ�ֵ���ɫ���壬��B�ǹ������ƣ�����D��������E��CO2��A��ˮ�����Է�Ӧ�ٵķ���ʽΪ2Na2O2+2H2O=4Na++4OH-+O2����������������Ԫ�صĻ��ϼ��ǣ�1�ۣ���������1mol����ת�Ƶ�����2NA��
�����Ѷȣ�һ��
2��ѡ���� X��Y��Z����ѧ��ѧ������������ɫ���ʣ�����ɵ�Ԫ�ؾ���������Ԫ�أ���Ħ�����������������Ǿ�����ˮ����������ԭ��Ӧ����ˮ�Ȳ���������Ҳ���ǻ�ԭ��������˵���������
A��X��Y����ʹʪ��ĵ��۵⻯����ֽ����
B��1molY��Z������ˮ��ȫ��Ӧʱ����ת��1mol����
C��ZΪ���ӻ���������й��ۼ������������Ӹ�����Ϊ1:2
D��X��Y�����������ſ���������ˮ���ռ�
�ο��𰸣�D
�������������ˮ����������ԭ��Ӧ����ˮ�Ȳ���������Ҳ���ǻ�ԭ������ɫ������Ҫ��NO2��Cl2��Na2O2������Ħ����������ȷ��XΪNO2��YΪCl2��ZΪNa2O2��X��Y������ǿ�����ԣ�������ʹʪ��ĵ⻯�ص�����ֽ������A��ȷ��1molY��Z��������ˮ������Ӧʱת�Ƶĵ�������Ϊ1mol��B��ȷ��ZΪ���ӻ��������Na+��O22-�����Ժ��й��ۼ������������Ӹ�����Ϊ1:2��C��ȷ��X����ˮ����3NO2+H2O=2HNO3 +NO�����Բ�������ˮ���ռ���D����ѡD��
����������Ϊ�ƶ��⣬��Ҫ����ѧ������������������ѶȽϴ�
�����Ѷȣ���
3������� ijЩ��ѧ��Ӧ������ʽ��ʾ��δ��ƽ����A+B��C+D+H2O����ش��������⣺
��1����A��C��D��������Ԫ�أ���A����Ԫ�صĻ��ϼ۽���C��D֮�䣬д���÷�Ӧ�����ӷ���ʽ��______��
��2����AΪ�Ϻ�ɫ������DΪ��ɫ�̼������壬��д��������ʽ�Ļ�ѧ����ʽ��______��
��3����C��D��Ϊ���壨����C����ɫ���ҷ��Ӿ�����ͬ��ԭ�Ӹ����ȣ��������ʽ��ѧ����ʽ�ǣ�______��
�ο��𰸣���1����A��C��D��������Ԫ�أ���A����Ԫ�صĻ��ϼ۽���C��D֮�䣬Ӧ���绯��Ӧ��������ǿ��ķ�Ӧ����ת����ϵ����Ӧ���ӷ���ʽΪ��Cl2+2OH-�TCl-+ClO-+H2O��
�ʴ�Ϊ��Cl2+2OH-�TCl-+ClO-+H2O��
��2��AΪ�Ϻ�ɫ������A��Cu������DΪ��ɫ�̼������壬Ӧ��Cu��Ũ���ᷴӦ��������ͭ������������ˮ����Ӧ����ʽΪ��Cu+2H2SO4��Ũ����.CuSO4+2H2O+SO2����
�ʴ�Ϊ��Cu+2H2SO4��Ũ����.CuSO4+2H2O+SO2����
��3����C��D��Ϊ���壨����C����ɫ���ҷ��Ӿ�����ͬ��ԭ�Ӹ����ȣ�Ӧ��̼��Ũ���ᷴӦ���ɶ�����̼������������ˮ����Ӧ����ʽΪ��Cʮ4HNO3��Ũ����.CO2��+4NO2��+2H2O��
�ʴ�Ϊ��Cʮ4HNO3��Ũ����.CO2��+4NO2��+2H2O��
���������
�����Ѷȣ�һ��
4������� ��A��B��C��D������ɫ���壬
��A��ʹʪ��ĺ�ɫʯ����ֽ������
��һ�������£�A������B��Ӧ����C��C��������Ϊ����ɫ��
��D��A������ɰ��̣�
��D��Ũ��Һ�����̿���Ҫ�ɷ���MnO2���ڼ��������·�Ӧ����ȡ����ɫ����E����Ҫ��ش��������⣺
��1��д���ڻ�ѧ����ʽ______��
��2��д���ܵ����ӷ���ʽ______��
��3������E�ж���ʵ����һ����______���գ��÷�Ӧ�����ӷ���ʽ��______��
�ο��𰸣���A��ʹʪ��ĺ�ɫʯ����ֽ�������ǰ������������ʣ��ж�ΪNH3��
��һ�������£�A������B��Ӧ����C��C��������Ϊ����ɫ������ɫ����ΪNO2���ж�CΪNO��
��D��Ũ��Һ�����̿���Ҫ�ɷ���MnO2���ڼ��������·�Ӧ����ȡ����ɫ����E���ƶ�DΪŨ���ᣬ����ɫ����EΪCl2��
��D��A������ɰ��̣�˵��AΪNH3��BΪO2����
���������жϳ�������Ϊ��AΪNH3��BΪO2��CΪNO��DΪHCl��EΪCl2��
��1����Ӧ���ǰ����Ĵ���������һ��������ˮ��һ�������Ϳ�����������Ӧ���ɺ���ɫ���������������Ӧ�Ļ�ѧ����ʽΪ��4NH3+5O2����.��4NO+6H2O��2NO+O2=2NO2
�ʴ�Ϊ��4NH3+5O2����.��4NO+6H2O��2NO+O2=2NO2��
��2����Ӧ����ʵ�����Ʊ������ķ�Ӧ�����Ȼ�þ��������ˮ����Ӧ�����ӷ���ʽΪ��MnO2+4H+?��?.?Mn2++Cl2��+2H2O���ʴ�Ϊ��MnO2+2Cl-+4H+?��?.?Mn2++Cl2��+2H2O��
��3������EΪ�����ж������ŷŵ���������Ⱦ��������Ҫ������������Һ���գ���Ӧ�����ӷ���ʽΪ��Cl2+2OH-=Cl-+ClO-+H2O���ʴ�Ϊ��NaOH��Һ��Cl2+2OH-=Cl-+ClO-+H2O��
���������
�����Ѷȣ�һ��
5������� ��12�֣�
���п�ͼ��ʾ���й�����֮���ת����ϵ�����з�Ӧ������P��Һ�е�ˮ��δ�������֪������D��E��F��H��L��N��Ϊ���壻A����ɫ��Ӧ�ʻ�ɫ����B����Һ�еμ�KSCN��Һ������������1molB���������ֽ�õ�F��G��H��������������ʵ�����Ϊ1mol��F������Ѫ�쵰��ϵ����ʣ�J���ִ������Ӧ����㷺�Ľ������ʡ�
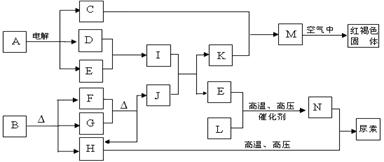
��ش������⣺
��1�����ɵ���J��Ԫ�������ڱ��е�λ����?��
��2��B�Ļ�ѧʽ?��? N�Ŀռ乹����?��
��3��д��M�ڿ����б�Ϊ���ɫ����Ļ�ѧ����ʽ?��
��4��D��E��Ӧ���Ƶ�һ����Ҫ�Ļ���ԭ��I���䷴Ӧ��������?��
��5��N��H�ڸ��¸�ѹ���ܺϳ�����[CO(NH2)2]���䷴Ӧ�Ļ�ѧ����ʽΪ?
?��
�ο��𰸣���12��
��1���������ڢ���?��2�֣�
��2��FeC2O4?����?����2�֣�
��3��4Fe(OH) 2+O2+2H2O==4Fe(OH)3?��2�֣�
��4����ɫ���棬�ų�������?��2�֣�
��5��2NH3 + CO2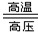 CO(NH2)2+ H2O?��2�֣�
CO(NH2)2+ H2O?��2�֣�
�����������
�����Ѷȣ�һ��