1��ѡ���� һ���ͳ�ҹ����ʻ�ڹ�·�ϣ���������©�ͣ���������������͵���ζ����ʱӦ�ò�ȡ��Ӧ����ʩ��
A����ˮ���²��ܽ���������
B�����Ʋ���©�Ͳ�λ����ʱ����
C���������Ͻ��̻���ɢ�˿��뿪����
D���ó�����Ա���ã���Ҫ�����߶�
�ο��𰸣�C
���������A�����Ͳ�����ˮ��A����ȷ��B�������������������������ը��B����ȷ��C��������ȼ�ױ�����˴������Ͻ��̻���ɢ�˿��뿪��������ȷ�ģ�C��ȷ��D���ó�����Ա���ã���Ҫ�����߶����ڴ����������D����ȷ����ѡC��
�����Ѷȣ���
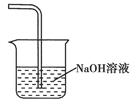
2��ѡ���� ��һֻ25 mL�ļ�ʽ�ζ�����ע��0��1 mol/L������������Һ����Һ��ǡ����5mL�Ŀ̶ȴ������ѵζ����е���Һȫ�������ձ��У���������Һ�����
A������20mL
B����20mL
C������20mL
D������5mL
�ο��𰸣�A
�������������ζ��ܵĽṹ��ʹ�÷�����
�����Ѷȣ���
3��ѡ���� ͭпԭ��أ���ͼ������ʱ�����������������
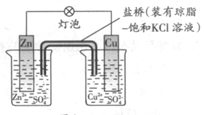
A.������ӦΪ��Cu2++2e�C= Cu
B.��ط�ӦΪ��Zn+Cu2+=Zn2+ +Cu
C.�����·�У����ӴӸ�����������
D.�����е�K+����ZnSO4��Һ
�ο��𰸣�D
������������������ͭпԭ�����п�ϻ���ʧȥ���ӷ���������Ӧ�Ǹ�����ͭ���õ����ӷ�����ԭ��Ӧ������������п�������ӣ�Zn2+ ��Խ��Խ�࣬Ϊ��ά����Һ�����ԣ����ŵ�Cl-������ZnSO4��Һ��������K+����ѡD
���㣺ԭ���
����������ԭ��صĻ�������ԭ�����ѶȲ������ڳ����⡣
�����Ѷȣ���
4��ʵ���� FeCl3���ִ���ҵ������Ӧ�ù㷺��ij��ѧ�о���ѧϰС��ģ�ҵ�����Ʊ���ˮFeCl3�����ø���ƷFeCl3��Һ�����ж���H2S��
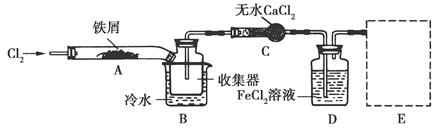
��.���������ϵ�֪����ˮFeCl3�ڿ������׳��⣬����������������������Ʊ���ˮFeCl3��ʵ�鷽����װ��ʾ��ͼ(���ȼ��г�װ����ȥ)�������������£�
�ټ���װ�õ������ԣ�
��ͨ������Cl2���Ͼ�װ���еĿ�����
���þƾ�������м�·���������Ӧ��ɣ�
�ܡ���
����ϵ��ȴ��ֹͣͨ��Cl2�����ø����N2�Ͼ�Cl2�����ռ����ܷ⡣
��ش��������⣺
(1)װ��A�з�Ӧ�Ļ�ѧ����ʽΪ______________��
(2)�ڢ۲����Ⱥ����ɵ���״FeCl3�ֽ����ռ��������������ڷ�Ӧ��A�Ҷˡ�Ҫʹ������FeCl3�����ռ������ڢܲ�������________��
(3)���������У�Ϊ��ֹFeCl3��������ȡ�Ĵ�ʩ��(������)________��
(4)װ��B����ˮԡ������Ϊ________��װ��C������Ϊ________��װ��D��FeCl2ȫ����Ӧ����ʧȥ����Cl2�����ö�ʧЧ��д������FeCl2�Ƿ�ʧЧ���Լ���________��
(5)�����߿��л���β������װ��E��ע���Լ���
��.����ͬѧ��װ��D�еĸ���ƷFeCl3��Һ����H2S���õ��������˺�����ʯīΪ�缫����һ�������µ����Һ��
(6)FeCl3��H2S��Ӧ�����ӷ���ʽΪ________________��
(7)������H���������ŵ����H2�������ĵ缫��ӦʽΪ____________________��
(8)�ۺϷ���ʵ����������Ӧ����֪��ʵ�������������ŵ㣺
��H2S��ԭ��������Ϊ100%����________________��
�ο��𰸣�(1)2Fe��3Cl2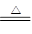 2FeCl3
2FeCl3
(2)�ڳ�����FeCl3�����·�����
(3)�ڢ�
(4)��ȴ��ʹFeCl3�����������ռ���Ʒ�������
K3[Fe(CN)6]��Һ
(5)
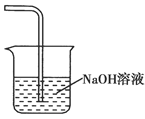
(6)2Fe3����H2S=2Fe2����S����2H��
(7)Fe2����e��=Fe3��
(8)FeCl3�õ�ѭ������
�������������FeCl3�����ʼ������Ʊ������֪ʶ���
(1)Cl2��Fe�ķ�ӦΪ3Cl2��2Fe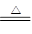 2FeCl3��(2)����FeCl3���������������ʣ����ԶԷ�Ӧ���г���FeCl3�IJ�λ���ȣ�ʹ��������(3)Ϊ�˷�ֹFeCl3���⣬�ڸϾ�װ���еĿ�������ֹˮ�������ڣ�����ȴʱҪ��Cl2����ȴ�����ø����N2�Ͼ�Cl2��(4)װ��B����ˮԡ�������ǽ�FeCl3������ȴΪFeCl3���塣װ��CΪ����ܡ�����
2FeCl3��(2)����FeCl3���������������ʣ����ԶԷ�Ӧ���г���FeCl3�IJ�λ���ȣ�ʹ��������(3)Ϊ�˷�ֹFeCl3���⣬�ڸϾ�װ���еĿ�������ֹˮ�������ڣ�����ȴʱҪ��Cl2����ȴ�����ø����N2�Ͼ�Cl2��(4)װ��B����ˮԡ�������ǽ�FeCl3������ȴΪFeCl3���塣װ��CΪ����ܡ�����
FeCl2�Ƿ�ʧЧ���Ǽ���D���Ƿ����Fe2����������K3[Fe(CN)6]��Һ���飬����������Fe2������Һ������ɫ�������ɡ�(5)Cl2���ж����壬�����ü�Һ���գ�����ͼ��ʾ��(6)H2S��FeCl3����������ԭ��Ӧ��2Fe3����H2S=2Fe2����S����2H����(7)��Ϊ��������Ϊʯī������������Һ�е�Fe2���ŵ磺Fe2����e��=Fe3����(8)ʵ���������ŵ��Ǣ�H2S�������ʸߣ���FeCl3����ѭ�����á�
�㲦��֪ʶ�����ʵ��Ʊ���β���Ĵ��������ӵļ���Ȼ�ѧʵ��֪ʶ�����ӷ���ʽ�͵缫��Ӧʽ����д�����������ؿ���ѧ���������������������������Ѷȣ��еȡ�
�����Ѷȣ�һ��
5��ѡ���� ��100����ijһԪ���ᣨKa��10��3��10��7������Һ�У���0.50mol/L����������Һ�ζ���õζ���������ͼ��ʾ������������ȷ���ǣ�
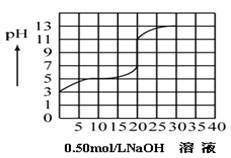
A���������ڵζ�ǰ��Ũ����0.15 mol/L��
B��������ĵ��볣��(Ka)��10��5
C���ڵζ����̣�Ϊ��ζ��յ㣬����ʵ�ָʾ���Ƿ�̪
D���ڵζ����̣�Ϊ��ζ��յ㣬����ʵ�ָʾ���Ǽ���
�ο��𰸣�BC
����������ɿ�������к�ʱ�����ĵļ�Һ�����Ϊ20ml�����ᣨ����ΪHA����Ũ��Ϊc mol/L����0.1c=0.5��0.02��c=0.1mol/L��A����ȷ
ԭ����ҺpH=3,��HA H����A����H����A����Ũ�Ⱦ�Ϊ10��3 mol/L���ɵ���ƽ�ⳣ����Ka=
H����A����H����A����Ũ�Ⱦ�Ϊ10��3 mol/L���ɵ���ƽ�ⳣ����Ka=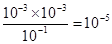 ��B��ȷ
��B��ȷ
����ǡ���к�ʱ���ɵ�������ǿ������Һ���ʼ��ԣ�����Ҽ��������µı�ɫ��ָʾ����Ҳ���Ƿ�̪�Լ���C��ȷ���ų�D
�ʴ�ΪBC
�����Ѷȣ�һ��