1、填空题 请从图中选用必要的装置进行电解饱和食盐水的实验,要求测定产生的氢气的体积(大于25mL),并检验氯气的氧化性。
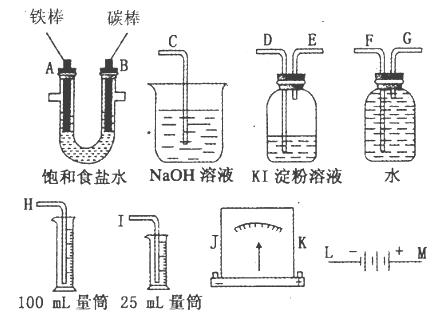
(1)A极发生的电极反应式是_____________________・B极发生的电极反应式是_______________________;电解饱和食盐水的化学方程式是______________________。
(2)电源的M端应连接的电极为____________(A或B)极。
(3)设计上述气体实验装置时,各接口的正确连接顺序为:______________________________
__________________________________(填接口编号)。
(4)实验中,在盛有KI淀粉溶液的容器中发生反应的离子方程式为________________。
(5)已知饱和食盐水50mL,某时刻测得H2体积为56mL(标准状况)。此时溶液pH约为___________________。
参考答案:(1)2 H++2e-=H2↑;(2分) 2 Cl--2e-= Cl2↑(2分)
2NaCl+2H2O 2NaOH+ H2↑+ Cl2↑(2分)
2NaOH+ H2↑+ Cl2↑(2分)
(2)B(2分)
(3)H、F、G、A、B、D、E、C(2分)
(4)Cl2+2I-="2" Cl-+2I2(2分)
(5)13(2分)
本题解析:(1)A极应作阴极,H+放电,电极反应式是2 H++2e-=H2↑,B极是阳极,Cl-放电,电极反应式是2 Cl--2e-= Cl2↑电解饱和食盐水的化学方程式是2NaCl+2H2O 2NaOH+ H2↑+ Cl2↑;
2NaOH+ H2↑+ Cl2↑;
(2)M是正极应连接阳极B极,
(3)收集氢气用排水集气法,所以A→G→F→H,验证氯气的氧化性用淀粉碘化钾溶液,剩余氯气用氢氧化钠溶液吸收,所以B→D→E→C,整体连起来为H、F、G、A、B、D、E、C;
(4)在盛有KI淀粉溶液的容器中发生反应是氯气置换碘的反应,离子方程式为Cl2+2I-="2" Cl-+2I2
(5)n(H2)=0.0025mol,所以n(NaOH)=0.005mol,c(NaOH)=0.1mol/L,pH=13.
本题难度:一般
2、选择题 海带中的碘元素是以I-的形式存在的,为将I-转化成I2并提取出来,设计操作步骤如下:①通入Cl2;②将海带烧成灰,向灰中加水,搅拌;③加CCl4振荡;④过滤;⑤用分液漏斗分液。合理的操作顺序为(?)
A.①③⑤②④
B.②①③④⑤
C.②④①③⑤
D.③①②⑤④
参考答案:C
本题解析:从海带中提取碘单质的操作为:先将海带烧成灰,向灰中加水搅拌;再过滤,向滤液通入Cl2,然后加CCl4振荡,最后用分液漏斗分液,合理的操作顺序为②④①③⑤,选C。
本题难度:一般
3、选择题 非金属氧化物在下列反应中不表现为酸性氧化物性质的是
A.SO2+Na2SO3+H2O==2NaHSO3
B.Ca(ClO)2+CO2+H2O==CaCO3+2HclO
C.SO2+H2O2==H2SO4
D.P2O5+3CaO==Ca3(PO4)2
参考答案:C
本题解析:略
本题难度:简单
4、选择题 下列物质中,分别加入少量溴水,振荡后静置,溶液无色的是( ?)
A.NaOH溶液
B.NaCl
C.KI溶液
D.Zn粉
参考答案:AD
本题解析:
正确答案:AD
A、2NaOH+Br2=NaBr+NaBrO+H2O, NaBr和NaBrO均呈无色
B、不反应;
C、2KI+Br2=I2+2KBr,碘水呈黄色
D、Zn+Br2=ZnBr2,溶液呈无色。
本题难度:简单
5、简答题 在实验室里制取少量FeCl3,可按照一定顺序连接下图中所列装置,所通过的气体过量且反应充分.试回答以下问题:
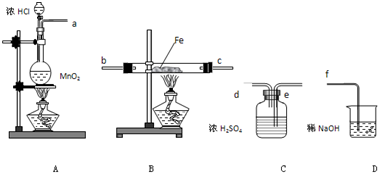
(1)实验时,各装置接口的连接顺序为______(用a、b、c、d等字母表示);
(2)C装置的作用是______;
(3)D装置的作用是______;
(4)检验B装置中反应后铁是否有剩余的方法是:______;
(5)用此方法可制得无水氯化铁.你认为能否改用Fe和盐酸反应,再通入过量氯气、蒸干溶液的方法来制取无水氯化铁,______(答:是或否);说明理由:______.
参考答案:(1)制备氯气中含有氯化氢和水蒸气,有水蒸气不能制的氯化铁,除去水蒸气用浓硫酸,应先除去水蒸气干燥,干燥的氯气通入玻璃管中和铁反应生成无水氯化铁,最后吸收尾气中未反应的氯气,防止污染空气,洗气装置导气管长进短处,导气管口连接顺序为:a?e?d?b?c?f,故答案为:a e d b c f;
(2)气体中含有水蒸气,FeCl3容易水解,C装置中是浓硫酸作用是干燥氯气,故答案为:干燥氯气;
(3)氯气有毒不能排放到空气中,氢氧化钠作用是吸收尾气氯气,防止污染空气,故答案为:吸收尾气氯气;
(4)检验B装置中反应后铁是否有剩余的方法是,用磁铁吸引产物,若被磁铁吸引,则含有铁,
故答案为:用磁铁吸引产物,若被磁铁吸引,则含有铁;
(5)改用Fe和盐酸反应生成氯化亚铁,再通入过量氯气把氯化亚铁氧化为氯化铁,因为氯化铁水解,蒸干溶液,得到的是氢氧化铁;不能来制取无水氯化铁,
故答案为:否;由于FeCl3?水解,加热蒸干该溶液只能得到Fe(OH)3.
本题解析:
本题难度:一般