1、选择题 下列说法正确的是(?)
A.H2O是一种非常稳定的化合物,这是由于氢键所致
B.稀有气体形成的晶体属于分子晶体
C.干冰升华时,分子内共价键会发生断裂
D.金属晶体的熔点普遍都很高
参考答案:B
本题解析:氢键一般影响物质的物理性质,水分子稳定,是由于化学键的原因。干冰升华属于物理变化,破坏的是分子间作用力。金属晶体的熔点并不都是普遍很高,例如碱金属等。所以正确的答案是B。
本题难度:一般
2、填空题 W、X、Y、Z是原子序数依次增大的同一短同期元素,W、X是金属元素,Y、Z是非金属元素.
(1)W、X各自的最高价氧化物对应的水化物可以反应生盐和水,该反应的离子方程式为______.
(2)W与Y?可形成化合物W2Y,该化合物的电子式为______.
(3)Y的低价氧化物通入Z单质的水溶液中,发生反应的化学方程式为______.
(4)比较Y、Z气态氢化物的稳定性______>______(用分子式表示).
(5)Y、Z四种元素简单离子的离子半径由大到小的顺序是______>______>______>______.
参考答案:(1)W、X为金属,其最高价氧化物对应的水化物为碱,且两种碱可以反应生成盐和水,则为NaOH和Al(OH)3,二者反应的离子方程式:Al(OH)3+OH-=AlO2-+2H2O,故答案为:Al(OH)3+OH-=AlO2-+2H2O;(2)W为Na,W可以和Y形成W2Y,则Y为-2价,为ⅥA元素,且和钠同周期,所以为S.W2Y为Na2S,电子式为:
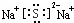
,故答案为:
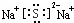
;
(3)Y的低价氧化物为SO2;并且Z和Y同周期,原子序数比Y大,所以Y为Cl.Y的低价氧化物和Z的单质反应的方程式:SO2+Cl2+2H2O=H2SO4+2HCl,故答案为:SO2+Cl2+2H2O=H2SO4+2HCl;
(4)非金属性越强,气态氢化物的稳定性越强;由于非金属性:Cl>S,所以气态氢化物的稳定性:HCl>H2S,故答案为:HCl>H2S.
本题解析:
本题难度:一般
3、选择题 甲醛分子式为CH2O,有强烈刺激性气味的气体,甲醛在常温下是气态,被世界卫生组织确定为致癌和致畸形物质。下列关于其结构及性质的分析正确的是(?)
A.C原子采取sp3杂化,O原子采取sp杂化
B.甲醛分子中心原子价层电子对数为4,含有一对孤电子对,是三角锥形结构
C.甲醛分子与水分子间可以形成氢键,甲醛分子间不能形成氢键
D.甲醛分子为非极性分子
参考答案:C
本题解析:甲醛是平面型结构,碳原子是sp2杂化,属于极性分子,选项ABD都是错误的,C正确,答案选C。
本题难度:简单
4、填空题 化合物A是一种不稳定的物质,它的分子组成可用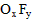 表示,10mL A气体能分解生成15mLO2和10mLF2
表示,10mL A气体能分解生成15mLO2和10mLF2
(同温同压下)
(1)A的分子式___________________;
(2)已知A分子中X个氧原子是…-O-O-O-…链状排列,则A分子的电子式____________________,结构式是_____________________。
参考答案:(1)O3F2
(2)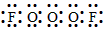 ;F-O-O-O-F
;F-O-O-O-F
本题解析:
本题难度:一般
5、简答题 元素周期表是学习化学的重要工具.下表为8种元素在周期表中的位置.
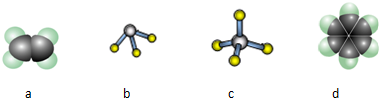
(1)下图所示的模型表示的分子中,可由A、D形成的是______(填选项序号).
(2)比较M、R元素的非金属性:______>______(填元素符号).
(3)Q元素在周期表中的位置是第______周期______族,其原子结构示意图为______.
(4)Na在R的单质气体中燃烧产物的电子式为______,Na在F单质中燃烧的产物是______(填化学式).
(5)上述元素的最高价氧化物的水化物中,碱性最强的是______(填化学式),其与Q的单质反应的离子方程式是______.
(6)比较Na、G、Q?3种元素的金属性:Na>______>______(填元素符号),能证明其金属性强弱的实验依据是______.
参考答案:根据元素所在周期表中的位置可知A为H元素,D为C元素,F为O元素,G为Mg元素,Q为Al元素,M为S元素,R为Cl元素,N为K元素,
(1)A为H元素,D为C元素,二者形成的化合物为烃,题中a为C2H4,b为NH3,c为CH4,d为C6H6,
故答案为:acd;
(2)M为S元素,R为Cl元素,同周期元素从左到右元素的非金属性逐渐增强,则非金属性:Cl>S,
故答案为:Cl;S;
(3)Q为Al元素,原子核外有3个电子层,最外层电子数为3,原子结构示意图为
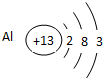
,位于周期表第三周期ⅢA族,
故答案为:三;ⅢA;
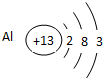
;
(4)Na在Cl2中燃烧生成NaCl,为离子化合物,电子式为
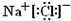
,Na在O2中燃烧生成Na2O2,
故答案为:
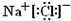
;Na2O2;
(5)金属性最强的元素为第四周期ⅠA族元素K,对应最高价氧化物的水化物KOH的碱性最强,与Al反应的离子方程式为
2Al+2OH-+2H2O=2AlO-2+3H2↑,
故答案为:KOH;2Al+2OH-+2H2O=2AlO-2+3H2↑;
(6)金属性强弱,可根据金属单质与水或酸反应的剧烈程度判断,同周期元素从左到右元素的金属性逐渐减弱,则金属性:Na>Mg>Al,
故答案为:Mg;Al;比较与水或与酸反应置换出氢气的难易程度(或比较最高价氧化物对应的水化物的碱性强弱).
本题解析:
本题难度:一般