1、选择题 我国首创的海洋电池以铝板为负极,铂网为正极,海水为电解质溶液,空气中的氧气与铝反应产生电流。电池总反应为:4Al+3O2+6H2O=4Al(OH)3,下列说法不正确的是
[? ]
A. 正极反应式为:O2+2H2O+4e-=4OH-
B. 电池工作时,电流由铝电极沿导线流向铂电极
C. 以网状的铂为正极,可增大与氧气的接触面积
D. 该电池通常只需更换铝板就可继续使用
参考答案:B
本题解析:
本题难度:一般
2、选择题 如图所示,用铁棒和石墨棒作电极电解1L 1mol/L食盐水,下列有关说法 ?正确的是 (? )
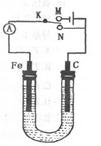
A.电键K与N连接,铁棒被保护而免受腐蚀
B.电键K与N连接,正极反应式为:4OH--4e-=2H2O +O2 ↑
C.电键K与M连接,将石墨棒换成铜棒,就可实现在铁棒上镀铜
D.电键K与M连接,当两极共产生标准状况下气体33.6L时,理论上生成lmol NaOH
参考答案:D
本题解析:A.电键K与N连接,构成的是原电池,Fe的活动性比C强,作负极,被氧化而受腐蚀。错误。B.电键K与N连接,构成的原电池中由于NaCl溶液是中性介质,发生的是吸氧腐蚀。正极反应式为: O2 +4e-+2H2O =4OH-。错误。C.电键K与M连接,形成的是电解池。将石墨棒换成铜棒,铜棒作阳极,被氧化为Cu2+进入溶液,在阴极Fe上,2H++2e-=H2↑..错误。D.电键K与M连接,形成的是电解池,电解食盐水。n(气体)=1.5mol.反应的方程式为:2NaCl+2H2O 2NaOH+ H2↑+Cl2↑。n(NaCl)=1mol.所以当阳极产生n(Cl2)=0.5mol,阴极产生气体n(H2)=0.5mol时,NaCl消耗完全,这时的反应改为电解NaOH溶液,实质是电解水。2H2O
2NaOH+ H2↑+Cl2↑。n(NaCl)=1mol.所以当阳极产生n(Cl2)=0.5mol,阴极产生气体n(H2)=0.5mol时,NaCl消耗完全,这时的反应改为电解NaOH溶液,实质是电解水。2H2O 2H2↑+O2↑。NaOH的物质的量不变。根据元素守恒可得理论上生成lmol NaOH。正确。
2H2↑+O2↑。NaOH的物质的量不变。根据元素守恒可得理论上生成lmol NaOH。正确。
本题难度:一般
3、选择题 如图有关电化学的图示,完全正确的是( )
A.
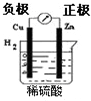
Cu-Zn原电池
B.
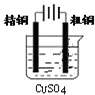
粗铜的精炼
C.
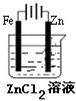
铁片镀锌
D.

验证NaCl溶液(含酚酞)电解产物
参考答案:A、原电池中较活泼的金属作负极,较不活泼的金属或导电的非金属作正极,所以铜-锌-稀硫酸原电池中,锌作负极铜作正极,故A错误;
B、粗铜的精炼中,粗铜作阳极,纯铜作阴极,电解质溶液为含有铜离子的盐,故B错误;
C、电镀时,镀层作阳极,镀件作阴极,所以铁片上镀锌,锌作阳极,铁作阳极,故C错误;
D、电解时,电流流入的电极为阳极,另一电极为阴极,所以电解氯化钠溶液时,根据图片知,碳棒为阳极,铁棒为阴极,阳极上氯离子失电子生成氯气,氯气能置换碘化钾中的碘,碘遇淀粉变蓝色,所以阳极上用淀粉碘化钾溶液可检验氯气的存在;阴极上氢离子得电子生成氢气,利用氢气的燃烧实验检验阴极产物;溶液中有氢氧化钠产生,无色酚酞试液遇碱变红色,所以可用无色酚酞检验氢氧化钠的生成,故D正确;
故选D.
本题解析:
本题难度:一般
4、简答题 如图所示,甲、乙两池电极材料都是铁棒和碳棒,请回答下列问题:
(1)若两池中均为CuSO4溶液,反应一段时间后:
①有红色物质析出的是甲池中的______棒,乙池中的______棒.
②乙池中阳极的电极反应式是______.
(2)若两池中均为饱和NaCl溶液:
①写出乙池中总反应的离子方程式______.
②甲池中碳极上电极反应式是______,乙池碳极上电极反应属于______(填“氧化反应”或“还原反应”).
③若乙池转移0.02mol?e-后停止实验,池中溶液体积是200mL,则溶液混合均匀后的所得NaOH溶液的物质的量浓度为______.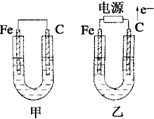
参考答案:(1)①甲池为原电池,原电池中活泼金属做负极,发生氧化反应,碳棒做正极,有Cu析出,乙池为电解池,外电路电子流向电源正极,所以碳棒为阳极,放出氯气,阴极铁电极上发生还原反应有Cu析出,故答案为:碳;铁;
②乙池中,惰性电极为阳极,电解硫酸铜溶液,阳极氢氧根离子放电生成氧气,电极反应为4OH--4e-=2H2O+O2↑,故答案为:4OH--4e-=2H2O+O2↑;
(2)①若电解质溶液为饱和氯化钠溶液,则乙池就是用惰性电极为阳极电解氯化钠溶液,方程式为:2NaCl+2H2O?通电?.?Cl2↑+H2↑+2NaOH,
故答案为:2NaCl+2H2O?通电?.?Cl2↑+H2↑+2NaOH;
②甲池中碳棒为正极,发生还原反应,氧气得到电子生成氢氧根,与吸氧腐蚀的电极反应相同,O2+2H2O+4e-=4OH-,乙装置中,碳棒是阳极,发生失电子的氧化反应,
故答案为:O2+2H2O+4e-=4OH-;氧化反应;
③电解氯化钠溶液的方程式为:2NaCl+2H2O?通电?.?Cl2↑+H2↑+2NaOH,乙池转移0.02mole-后,会生成0.02mol的氢氧化钠,所以所得NaOH溶液的物质的量浓度c=nV=0.02mol0.2L=0.1mol/L,故答案为:0.1mol/L.
本题解析:
本题难度:一般
5、选择题 右图中,两电极上发生的电极反应分别为:a极:Ag++e-=Ag,b极:Fe-2e-=Fe2+
下列说法正确的是(? )
A.a、b一定是两种不同的电极材料
B.装置中电解质溶液一定含有Ag+
C.装置中发生的反应可能是Fe2++2Ag Fe+2Ag+
Fe+2Ag+
D.该装置一定是电解池