1、简答题 在高温高压下CO具有极高的化学活性,能与多种单质或化合物反应。
(1)若在恒温恒容的容器内进行反应C(s)+H2O(g) CO(g)+H2(g),则可用来判断该反应达到平衡状态的标志有 ??。(填字母)
CO(g)+H2(g),则可用来判断该反应达到平衡状态的标志有 ??。(填字母)
a.容器内的压强保持不变? b.容器中H2浓度与CO浓度相等
c.容器中混合气体的密度保持不变? d.CO的生成速率与H2的生成速率相等
(2)CO一空气燃料电池中使用的电解质是搀杂了Y2O3的ZrO2晶体,它在高温下能传导O2?。该电池负极的电极反应式为??。
(3)一定条件下,CO与H2可合成甲烷,反应方程式为:CO(g)+3H2(g)  CH4(g)+ H2O (g)
CH4(g)+ H2O (g)
①一定条件下,该反应能够自发进行的原因是??。
②已知H2(g)、CO(g)和 CH4(g)的燃烧热分别为285.8 kJ・mol-1、283.0 kJ・mol-1和890,0 kJ・mol-1。
写出CO与H2反应生成CH4和CO2的热化学方程式:??。
(4)工业上可通过甲醇羰基化法制取甲酸甲酯,反应方程式为:?.
CH3OH(g)+CO(g) HCOOCH3(g)?△H=-29.1 kJ・mol-1
HCOOCH3(g)?△H=-29.1 kJ・mol-1
科研人员对该反应进行了研究.部分研究结果如下:

①从反应压强对甲醇转化率的影响“效率"看,工业制取甲酸甲酯应选择的压强是 ??。
②实际工业生产中采用的温度是80℃,其理由是??。
参考答案:
(1)ac?
(2)CO一2e一+O2一=CO2?
(3)①该反应△H<0
②2CO(g)+2H2(g) CH4(g)+C02(g)?△H="-247.6" kJ・mol-1
CH4(g)+C02(g)?△H="-247.6" kJ・mol-1
(4)①3.5×106 Pa~4.0×106 Pa
②高于80℃时,温度对反应速率影响较小;且反应放热,升高温度时平衡逆向移动,转化率降低
(每空2分,本题共12分)
本题解析:(1)“变量不变达平衡”,随反应进行体系中压强、密度(气体的质量发生变化)均是变量,b、物质的浓度不变是平衡标志,但相等只是一种特定状态,不可以;d、CO的生成速率与H2的生成速率相等同向,一定相等;(2)负极CO失去电子,生成CO2,CO一2e一+O2一=CO2 ;(3)①该反应的△S<0,只能△H<0才能自发进行;②2CO(g)+2H2(g) CH4(g)+C02(g)?△H="-247.6" kJ・mol-1;(4)①由图可知,当压强达到4.0×106 Pa压强对转化率的影响较小,故工业制取甲酸甲酯应选择的压强在3.5×106 Pa~4.0×106 Pa;②由图观察可知温度高于80℃时,温度对反应速率影响较小;且反应放热,升高温度时平衡逆向移动,转化率降低。
CH4(g)+C02(g)?△H="-247.6" kJ・mol-1;(4)①由图可知,当压强达到4.0×106 Pa压强对转化率的影响较小,故工业制取甲酸甲酯应选择的压强在3.5×106 Pa~4.0×106 Pa;②由图观察可知温度高于80℃时,温度对反应速率影响较小;且反应放热,升高温度时平衡逆向移动,转化率降低。
本题难度:困难
2、选择题 下列说法正确的是( )
A.铅蓄电池放电时铅电极发生还原反应
B.电解饱和食盐水在阳极得到氯气,阴极得到金属钠
C.给铁钉镀铜可采用CuSO4作电镀液
D.生铁浸泡在食盐水中发生析氢腐蚀
参考答案:A.铅蓄电池放电时铅电极为原电池的负极,发生氧化反应,正极发生还原反应,故A错误;
B.电解饱和食盐水得到氢气、氯气和氢氧化钠,阴极上得到氢气和氢氧化钠,故B错误;
C.电镀时用含镀层金属的阳离子的盐做电解质溶液,则给铁钉镀铜可采用CuSO4作电镀液,故C正确;
D.生铁浸泡在食盐水中发生吸氧腐蚀,在酸性溶液中发生析氢腐蚀,故D错误.
故选C.
本题解析:
本题难度:一般
3、选择题 下列说法不正确的是(?)
A.水解反应NH4++H2O NH3・H2O+H+达到平衡后,升高温度平衡正向移动
NH3・H2O+H+达到平衡后,升高温度平衡正向移动
B.在硫酸钡悬浊液中加入足量饱和Na2CO3溶液,振荡、过滤、洗涤,沉淀中加入盐酸有气体产生,该现象不足以说明Ksp(BaSO4)与Ksp(BaCO3)大小关系。
C.明矾水解生成Al(OH)3胶体,可用作净水剂
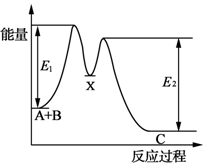
D.如图所示的反应过程中A+B→X的△H<0,X→C的△H>0