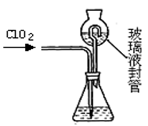
1、填空题 在新制的氯水参加的反应中,有如下几种情况:
(1)向KBr溶液中加入氯水,氯水中起作用的主要微粒是______,反应的离子方程式是______.
(2)向AgNO3溶液中加入氯水,氯水中起作用的主要微粒是______,反应的离子方程式是______.
(3)向氯水中滴加石蕊试液,溶液变红,起作用的微粒是______,然后又褪色,起作用的微粒是______.
参考答案:氯水含有H2O、Cl2、HClO、Cl-、H+、OH-,
(1)向KBr溶液中加入氯水,发生Cl2+2Br-=Br2+2Cl-,故答案为:Cl2;Cl2+2Br-=Br2+2Cl-;
(2)向AgNO3溶液中加入氯水,生成白色沉淀,发生Cl-+Ag+=AgCl↓,故答案为:Cl-;Cl-+Ag+=AgCl↓;
(3)氯气与水发生Cl2+H2O?HCl+HClO,具有酸性,向氯水中滴加石蕊试液,溶液变红,由于次氯酸具有漂白性,则加入试纸最终变为无色,故答案为:H+;HClO.
本题解析:
本题难度:一般
2、计算题 取含MnO2的软锰矿石11.6 g跟足量浓盐酸反应(杂质不参与反应),制得2.2 4 L Cl2(标准状况),求:
4 L Cl2(标准状况),求:
(1)这种软锰矿石中MnO2的百分含量。
(2)被氧化的HCl为的质量。
参考答案:(1)75%?(2)7.3g
本题解析:略
本题难度:一般
3、选择题 已知常温下氯酸钾与浓盐酸反应能放出氯气,现按右下图进行氯气的性质实验。玻璃管内分别装有滴有少量不同溶液的白色棉球,反应―段时间后,对图中指定部位颜色描述正确的是
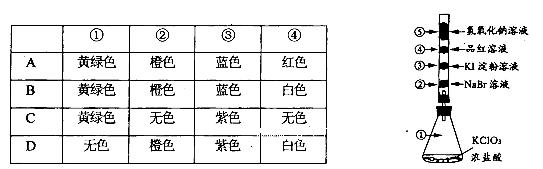
参考答案:B
本题解析:常温下氯酸钾与浓盐酸反应放出Cl2,①处充满黄绿色Cl2;氯气进入玻璃管后与②处NaBr溶液发生置换反应生成Br2,白色棉球变为橙色;氯气和③处KI溶液反应置换出I2,遇淀粉变蓝;④处利用氯气与碱液反应进行Cl2的尾气吸收,尽管反应生成的物质均为无色,但棉球本身是白色的,所以④处的颜色为白色2的制备、性质和溴、碘单质的性质
本题难度:一般
4、选择题 下列说法错误的是( )
A.Fe在Cl2中燃烧能生成FeCl3
B.氯化氢气体与氨气相遇,有大量的白烟生成
C.向蔗糖中加入浓硫酸,浓硫酸主要表现出脱水性和强氧化性
D.过量的铜和少量的稀硝酸充分反应后,再加入一定量稀硫酸,剩余铜片的质量不变
参考答案:A、氯气有强氧化性,能把变价金属氧化成最高价,所以氯气和铁反应生成氯化铁,故A正确.
B、烟是固体小颗粒,雾是液体小液滴,氯化氢气体与氨气相遇,生成氯化铵固体,所以有大量的白烟生成,故B正确.
C、浓硫酸具有酸性、吸水性、脱水性、强氧化性,蔗糖中含有C、H、O三种元素,浓硫酸能把蔗糖中的H、O元素按2:1的比例以水分子的形式脱去,最后把蔗糖氧化成单质C,所以浓硫酸主要表现出脱水性和强氧化性,故C正确.
D、铜和硝酸生成硝酸铜,硝酸铜电离出自由移动的硝酸根离子,加入稀硫酸后,溶液中有氢离子和硝酸根离子,相当于又有了硝酸,所以铜又能溶解,故D错误.
故选D.
本题解析:
本题难度:简单
5、实验题 .(16分)二氧化氯(ClO2)是目前国际上公认的第四代高效、无毒的广谱消毒剂,是一种黄绿色的气体,易溶于水。
Ⅰ.(1)ClO2可由KClO3在H2SO4存在的条件下与Na2SO3反应制得。则该反应的氧化产物与还原产物的物质的量之比是 。
Ⅱ.实验室也可用NH4Cl、盐酸、NaClO2(亚氯酸钠)为原料制备ClO2的流程如下:
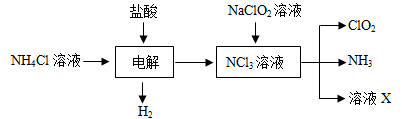
(2)写出电解时发生反应的化学方程式:?;
(3)除去ClO2中的NH3可选用的试剂是?;(填序号)
A.饱和食盐水
B.碱石灰
C.浓硫酸
D.水