1、选择题 下列物质不能与氢氧化钠溶液反应的是
A.Fe2O3
B.Al(OH)3
C.NaHCO3
D.H2SiO3
参考答案:A
本题解析:分析:根据碱的化学性质(能与酸反应生成盐和水、能与盐反应生成新盐和新碱)进行分析判断即可.
解答:A、氧化铁能与氢氧化钠溶液不会反应,故A正确;
B、氢氧化铝能和氢氧化钠反应生成偏铝酸钠溶液,可以发生反应,故B错误;
C、碳酸氢钠可以和氢氧化钠发生反应生成碳酸钠和水,可以发生反应,故C错误;
D、硅酸可以和氢氧化钠反应生成硅酸钠和水,可以反应,故D错误.
故选A.
点评:本题难度不大,考查氢氧化钠的性质,掌握碱的化学性质是正确解答本题的关键.
本题难度:困难
2、选择题 下列物质不能使溴水层褪色的是
A.镁粉
B.苯
C.苯乙烯
D.碘化钾
参考答案:D
本题解析:镁与溴水反应得到溴化镁无色溶液,苯可以发生萃取使水层无色,苯乙烯可以和溴水发生加成反应,得到无色溶液.而碘化钾与溴水发生置换反应以后,得到的碘水也有颜色.
本题难度:一般
3、选择题 在氧化还原反应3S+6KOH=K2SO3+2K2S+3H2O中,被氧化和被还原的物质的物质的量之比为
A.2:1
B.1:2
C.1:1
D.3:2
参考答案:B
本题解析:分析:在3S+6KOH=K2SO3+2K2S+3H2O反应中,硫元素化合价由0价升高为+4价,被氧化,硫元素由0价降低为-2价,被还原,所以硫既作氧化剂又作还原剂,根据还原产物与氧化产物的化学计量数进行判断.
解答:在3S+6KOH=2K2S+K2SO3+3H2O反应中,硫元素化合价由0价升高为+4价,被氧化,氧化产物为K2SO3,硫元素由0价降低为-2价,被还原,还原产物为K2S,
所以硫既作氧化剂又作还原剂,氧化剂被还原生成还原产物,还原剂被氧化生成氧化产物,
根据氧化产物与还原产物的化学计量数可知被氧化和被还原的S的物质的量之比为1:2,
故选B.
点评:本题考查氧化还原反应概念与计算,难度不大,根据化合价判断氧化剂与还原剂、还原产物与氧化产物是关键,判断后也可根据电子转移守恒计算还原剂与氧化剂的物质的量之比.
本题难度:困难
4、选择题 下列物质不可能由同一种元素组成的是
A.单质
B.混合物
C.氧化物
D.同位素
参考答案:C
本题解析:分析:根据氧化物的概念可知,氧化物中必须有两种元素,其中一种是氧元素,则不可能有一种元素组成.
解答:A、单质是一种元素组成的,金属单质是由一种金属元素组成的单质,故A不选;
B、混合物中至少两种物质,对于同素异形体组成的混合物,只有一种元素,如氧气和臭氧组成的混合物,故B不选;
C、氧化物要有两种元素,则不可能有一种元素组成,故C选;
D、同位素是质子数相同,中子数不同的同一类原子,是同种元素,故D不选;
故选:C.
点评:根据物质的组成来判断物质的类别,是解题的关键,同时要注意特殊情况,如对于同素异形体组成的混合物,只有一种元素,如氧气和臭氧组成的混合物.
本题难度:一般
5、选择题 下列反应中得不到SO2气体的是
A.Na2SO3固体+浓H2SO4
B.一定条件下SO3分解
C.Na2SO3固体+浓HNO3
D.燃烧硫
参考答案:C
本题解析:HNO3具有强氧化性,而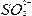 具有强还原性,HNO3将
具有强还原性,HNO3将![]() 氧化成
氧化成![]() 而不放出SO2。
而不放出SO2。
本题难度:困难