1、填空题 Ⅰ.A、B、C、D为前四周期元素。A元素的原子价电子排布为ns2np2,B元素原子的最外层电子数是其电子层数的3倍,C元素原子的M能层的p能级有3个未成对电子,D元素原子核外的M能层中只有2对成对电子。请回答下列问题:
⑴当n=2时,AB2属于_______分子(填“极性”或“非极性”),分子中有_______个π键。A6H6分子中A原子的杂化轨道类型是_______杂化。
⑵当n=3时,A与B形成的晶体属于_______晶体。
⑶若A元素的原子价电子排布为3s23p2,A、C、D三种元素的第一电离能由大到小的顺序是_______(用元素符号表示)。
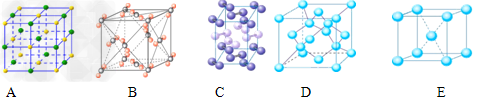
Ⅱ.⑴下列是钠、碘、金刚石、干冰、氯化钠晶体的晶胞图(未按顺序排序)。与冰的晶体类型相同的是__________(请用相应的编号填写)
⑵①与N2O互为等电子体的阴离子为______________(填一种即可);②根据价层电子对互斥模型确定ClO3-离子的空间构型为______________。
⑶已知某红紫色配合物的组成为CoCl3・5NH3・H2O,该配合物中的中心离子钴离子在基态时的核外电子排布式为___________。
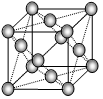
⑷下图是金属铝晶体结构的示意图。已知金属铝的密度为2.7g/cm3,则紧邻的铝原子的半径为_____________cm。(已知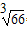 =4.04)?
=4.04)?
2、选择题 下列关于杂化轨道的叙述中,不正确的是
[? ]
A.分子中心原子通过sp3杂化轨道成键时,该分子不一定为正四面体结构
B.杂化轨道只用于形成σ键或用于容纳未参与成键的孤对电子
C.[Cu(NH3)4]2+和CH4两个分子的中心原子Cu 和C都是通过sp3杂化轨道成键
D.杂化轨道理论与VSEPR模型分析分子的空间构型结果常常相互矛盾
3、选择题 下列物质的化学用语正确的是( )
A.NH4H的电子式:
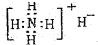
B.硝基苯的结构简式:

C.甲烷分子的比例模型:
D.sp2杂化轨道模型:

4、选择题 下列分子中,中心原子不是采取sp2型杂化的是( )
A.BCl3
B.PCl3
C.C2H4
D.C6H6
5、填空题 (三选一)【化学-物质结构与性质】
氯是一种非常重要的非金属元素。
(1)氯元素的基态原子的价电子层排布式是____________。
(2)氯化氢的沸点远低于氟化氢,液态氟化氢的化学式有时写成(HF)n,其原因是:
___________________
(3)光气(COCl2)中C原子采取_______杂化成键,其碳氧原子间的共价键含有_________(填“σ”或“π”键及个数)。
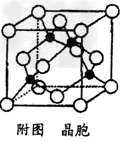
(4)元素Cu的一种氯化物的晶胞结构如图所示(黑球表示铜原子,白球表示氯原子),该氯化物的分子式____________,它可与浓氨水反应生成无色溶液,在空气中放置一段时间,最终溶液变成深蓝色,则深蓝色溶液中生成配合物为________________