1、填空题
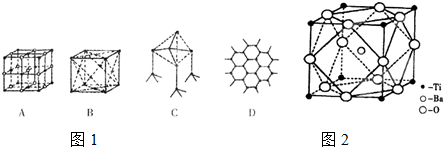
(1)图1所示一些晶体的结构(晶胞),其中代表干冰的是______;
(2)MgO晶胞空间构型与NaCl晶体相同,MgO晶体中Mg2+的配位数为______.与同个Mg2+等距且最近的O2-围成的空间几何构型是______.MgO晶体熔点高于NaCl晶体,原因是______;
(3)若C、D代表某种元素中的两种同分异构体,C中原子的杂化类型是______,属于______晶体.D中原子的杂化类型是______,D能导电的原因是______;
(4)原子晶体能否形成最密堆积结构?______,原因是______;
(5)偏钛酸钡的热稳定性好,介电常数高,在小型变压器、话筒和扩音器中都有应用.偏钛酸钡晶体中晶胞的结构示意图如
图2所示,它的化学式是______.
参考答案:(1)干冰是分子晶体,结合常见晶体可知,其中代表干冰的是B.
故答案为:B.
(2)根据氯化钠的配位数知,氧化镁晶体中镁离子的配位数是6;同个Mg2+等距且最近的O2-围成的空间几何构型是正八面体;电荷越大、离子半径越小其熔点越高,MgO晶体中离子的电荷数大于NaCl,离子间的平均距离小于NaCl,所以MgO晶体熔点高于NaCl晶体.
故答案为:6;正八面体;MgO晶体中离子的电荷数大于NaCl,离子间的平均距离小于NaCl.
(3)C中每个原子含有4个σ键,所以采取sp3杂化,该物质中构成了一个空间网状结构,所以属于原子晶体;
D中每个原子含有3个σ键,所以采取sp2杂化;导体能导电的原因是导体中含有在电流作用下能自由移动的电子,石墨是导体,每个碳原子上未参与杂化的一个2p轨道上电子在层内离域运动(石墨中有自由电子),所以能导电.
故答案为:sp3杂化、原子、sp2杂化、每个碳原子上未参与杂化的一个2p轨道上电子在层内离域运动(石墨中有自由电子).
(4)原子晶体中共价键有饱和性且配位数远小于12,所以不能形成最密堆积结构.
故答案为:不能;共价键有饱和性且配位数远小于12.
(5)该晶胞中含有一个钡原子,含有钛原子个数=8×18=1,含有氧原子个数=14×12=3,所以其化学式为BaTiO3.
故答案为:BaTiO3.
本题解析:
本题难度:简单
2、填空题 (1)氧化物MO与SiC属于等电子体,则M2+的核外电子排布式为____;MO的熔点比CaO的高,原因是___。
(2)K3[Fe(CN)6]晶体中含有的化学键类型为___;CN-中碳原子的杂化轨道类型是____,其电子式为____。
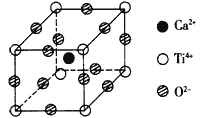
(3)金属钛被称为继铁和铝之后崛起的第三金属,如图为高温超导领域中 的一种化合物钙-钛矿(氧化物)晶体结构中具有代表性的最小重复 单元,在该晶体中每个钛离子周围与它最近且距离相等的钛离子有 ____个。该晶体的化学式为____。
参考答案:(1)1s22s22p6? ;Mg2+半径比Ca2+的小,MgO的晶格能大
(2)离子键、极性共价键、配位键;sp杂化 ;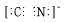
(3)6 ;CaTiO3
本题解析:
本题难度:一般
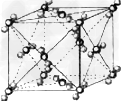
3、填空题 已知A、B、C、D、E、F都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E<F。其中B、D、F原子最外电子层的p能级(轨道)上的电子处于半满状态。通常情况下,A的一种氧化物分子为非极性分子,其晶胞结构如下图所示。E的电负性在该周期中最大。镓(Ga)与元素B形成的一种化合物是继以C单质为代表的第一代半导体材料和GaF为代表的第二代半导体材料之后,在近10年迅速发展起来的第三代新型半导体材料。?
试回答下列问题:(答题时,A、B、C、D、E、F用所对应的元素符号表示)
(1)基态Ga原子的核外电子排布式为________________。
(2)A、B、C的第一电离能由大到小的顺序为________。
(3)B元素的单质分子中有______个π键。
(4)上述A的氧化物分子中心原子采取______杂化,其晶胞中微粒间的作用力为______?
(5)FH3沸点与比BH3_____(填“高”或“低”),原因是________________。
(6)当0.01摩尔CrE3・6H2O在水溶液中用过量的AgNO3溶液处理时,常产生0.02摩尔的AgE沉淀,已知配离子配位数为6,此样品中配离子最可能是_______________。
参考答案:(1)1s22s22p63s23p63d104s24p1?
(2)N>C>Si?
(3)2?
(4)sp;范德华力
(5)低;NH3分子间能形成氢键,而AsH3分子间不能形成氢键
(6)[Cr(H2O)5Cl]2+
本题解析:
本题难度:一般
4、选择题 下列分子中的碳原子采取sp2杂化的是
[? ]
A.C2H2
B.C2H4
C.C3H8
D.CO2
参考答案:B
本题解析:
本题难度:简单
5、填空题 2011年是伟大的化学家、1954年诺贝尔化学奖得主、著名的化学结构大师、20世纪的科学怪杰鲍林(Linus Pauling)教授诞辰110周年(1901~ 1994)。1994年这位世纪老人谢世,人们打开他的办公室,发现里面有一块黑板,画得满满的,其中一个结构式如图,老人为什么画这个结构式?它是生命前物质吗?它有什么性质?这是鲍林留给世人的一个谜,也许这是一个永远无法揭开的谜,也许你有朝一日能揭开它。不管结果如何,让我们对这个结构式试作一番考察

(1)它的分子式是__________。
(2)它的所有原子是否处于同一个平面上?__________
(3)它是否带有电荷?____________。
(4)该分子中sp杂化的N原子有____个;sp2杂化的N原子有______个;sp3杂化的N原子有____个。
参考答案:(1)C6H2O2N10
(2)是
(3)否
(4)1;9;0
本题解析:
本题难度:一般