| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学知识点总结《电解池原理》高频考点预测(2019年最新版)(六)
参考答案:A 本题解析:用石墨做电极电解100mLH2SO4和CuSO4的混合液,首先发生反应:2CuSO4+2H2O 本题难度:一般 2、选择题 下列各组中,每种电解质溶液电解时只生成氢气和氧气的是 参考答案::C 本题解析::根据我们所学的电解原理,电解CuCl2时阳极析出氯气,阴极析出铜,A排除;电解CuSO4时阴极析出铜,排除B;电解NaBr时,阳极析出溴单质,D排除。 本题难度:一般 3、选择题 串联电路中的四个电解池分别装有0.1mol/L的下列溶液,用铂做电极,接通直流电源一段时间后,溶液pH最小的是( ) 参考答案:阳离子的放电顺序为:Ag+>Cu2+>H+>Na+>K+,阴离子的放电顺序为:I->Br->Cl->OH-, 本题解析: 本题难度:简单 4、简答题 (12分)D、A、B、C为四种原子序数依次增大的短周期元素,A、B、C同周期,A的原子半径是同周期中最大的;B、D同主族。已知D元素的一种单质是日常生活中饮水机常用的消毒剂,C元素的单质可以从A、B两元素组成的化合物的水溶液中置换出B元素的单质。 参考答案:(1)第三周期第ⅦA族; (2)碱性;S2-+H2O 本题解析:根据题意可知这几种元素分别是:A是Na;B是S;C是Cl;D是O。(1)Cl元素在周期表中的位置是位于第三周期第ⅦA族;(2)A、B元素形成的常见化合物Na2S是强碱弱酸盐,弱酸根离子水解使水溶液显碱性。水解的两种方程式为:S2-+H2O 本题难度:一般 5、选择题 用惰性电极电解一定浓度的CuSO4溶液时,通电一段时间后,硫酸铜有剩余,若想将溶液恰好恢复到电解前的浓度和pH(不考虑二氧化碳的溶解),则需加入下列哪种物质 |
参考答案:A
本题解析:电解CuSO4溶液时,发生:2CuSO4 + 2H2O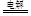 2Cu + O2↑+ 2H2SO4相当于原溶液中失去了Cu O,要恢复到原来的浓度,加入 CuO。
2Cu + O2↑+ 2H2SO4相当于原溶液中失去了Cu O,要恢复到原来的浓度,加入 CuO。
考点:电解池的应用。
本题难度:一般
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学试题《轨道表示式》考点.. | |