1、选择题 在无土栽培中,需配制一定量含50 molNH4Cl、6 molKCl和24 molK2SO4的营养液.若用KCl、NH4Cl和(NH4)2SO4三种固体为原料来配制,三者的物质的量依次是
A.2、54、24
B.54、2、24
C.32、50、12
D.16、50、24
参考答案:B
本题解析:根据形成溶液后离子的物质的量守恒,例:K+由6 molKCl,24 molK2SO4提供相当于54 molKCl提供.
本题难度:简单
2、选择题 下列各组物质中,可用溴水溶液来鉴别的是?(?)
A.乙烯与乙炔
B.乙烯与甲烷
C.苯与直馏汽油
D.苯与CCl4
参考答案:BD
本题解析:乙炔和乙烯都能和溴水发生加成反应,A不正确。甲烷和溴水不反应,所以选项B正确。苯和直馏汽油都和溴水不反应,C不正确。苯和四氯化碳都能和溴水发生萃取,其中苯在水的上层,四氯化碳在水的下层,D正确。答案选BD。
本题难度:一般
3、实验题 某化学兴趣小组同学在馓“证明海带中存在碘元素”的实验时,对课本上的描述:“海带灼烧后的灰烬中碘元素以I-形式存在”产生了疑问。久置KI固体被氧化变质,呈浅黄色(有I2),KI固体直接加热时,为什么不被氧化呢?因此,小组同学针对I-被氧化条件除了氧气之外还需要什么条件进行了实验探究。
【提出假设】根据久置KI固体会被氧化而变质,结合空气的成分,首先排除?和稀有气体的影响。然后对KI变质条件提出合理假设:
假设一:需要H2O的参与;
假设二:需要CO2的参与;
假设三:?。
【实验验证】
(1)为了验证假设二,小组同学设计了以下实验方案;取10mLKI溶液(浓度较大)于5支试管中,向试管中通入CO2气体或者滴加盐酸。一段时间后对比试管中的颜色深浅,之后向试管中滴入淀粉溶液,再次对比试管中的颜色深浅,具体实验现象见下表:
试管序号
| 1
| 2
| 3
| 4
| 5
|
通入CO2时间/min
| 0
| 1
| 5
| ?
| ?
|
滴加盐酸/滴
| 0
| ?
| ?
| 3
| 6
|
溶液中颜色对比
| 无色
| 浅黄色→黄色(依次加深)
|
滴加淀粉溶液后的颜色对比
| 无色
| 浅蓝色→蓝色(依次加深)
|
?
小组同学通过实验现象深入思考了CO2在反应过程中的作用,得出结论:CO2气体同盐酸一样在KI被氧化的过程中提供?环境。
写出此实验中CO2与KI反应的化学方程式?。
(2)为了验证I-被氧化是否必须要有H2O的参与,小组同学设计了以下实验验证:
实验步骤
| 预期现象和结论
|
①取一份纯净的KI固体,分成两等份;
| ?
|
②一份加入到装有?的集气瓶A中;
一份加入到装有?的集气瓶A中;
③几天后观察。
| ?
|
?
【交流提高】
由于空气中CO2和水蒸气的含量很低,导致在加热KI的过程中这两种气体很容易被“驱散”,不能很好地与KI接触,KI自然就不能被氧化。长时间保存碘化钾需要避光、?。
参考答案:(13分)
[提出假设]? N2(1分) ;? CO2、H2O的共同参与(2分);
[实验验证]?(1)酸性(1分);4KI + O2 + 2CO2 ="=" 2K2CO3 + 2I2(3分)
(2)
实验步骤:
预期现象和结论
①取一份纯净的KI固体,分成两等份;
?
②干燥的CO2和O2混合气体(1分)
潮湿的CO2和O2混合气体(1分)
若集气瓶A中的KI固体颜色变黄,则氧化KI可以不需要H2O参加(1分)。
若集气瓶A中的KI固体颜色不变,而集气瓶B的KI固体颜色变黄,则氧化KI必须要有H2O参加(1分)。
?
(合理叙述给分)
[交流提高]?密封且放置在干燥处(2分)
本题解析:本题的本质是对氧化条件的探究,发生反应的主体为碘离子和氧气,条件是H2O和CO2中的一种或两种,故探究的方向就是围绕H2O、CO2及H2CO3;从而设计实验进行证明。在实验过程中可以做对比实验和参照实验。在实验设计过程中,就是要对比有无H2O参与反应反应,故用CO2、O2与CO2、O2、H2O,二组反应进行对比从而得到结论。
在解题过程中要注意对题意的理解和与课本知识的结合,辅以解决这类问题的基本方程进行解答。这类题型要敢想、敢做,答题过程中力求准确、规范。
本题难度:一般
4、简答题 防止水体污染,改善水质,最根本的措施是控制工业废水和生活污水的排放.有一种工业废水,已知其中含有大量的Fe2+?和SO42-,少量的Ag+和Na+,以及部分污泥.某校化学兴趣小组同学通过下列操作过程,回收物质,处理废水.
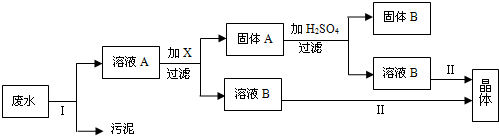
根据上述操作过程,回答下列问题:
(1)在实验室进行Ⅰ操作时,需要的主要玻璃仪器有______.
(2)操作Ⅱ的名称是______.
(3)向溶液A中需要加入过量X,X是______,发生反应的离子方程式为______.
(4)上述操作回收到的物质B是______,晶体是______.(两空均写名称)
参考答案:废水经过滤后可得含有大量的Fe2+?和SO42-,少量的Ag+和Na+的溶液,然后在滤液中加入过量Fe可置换出Ag,则固体A为Ag和Fe的混合物,加入硫酸可得硫酸亚铁溶液,固体B为Ag,则
(1)Ⅰ操作为过滤,需要的玻璃仪器有漏斗、烧杯、玻璃棒,故答案为:漏斗、烧杯、玻璃棒;
(2)溶液B为硫酸亚铁溶液,要得到硫酸亚铁晶体,应进行蒸发结晶操作,故答案为:蒸发结晶;
(3)由以上分析可知X为Fe,发生反应为Fe+2Ag+=Fe2++2Ag,可置换出Ag,进而回收,
故答案为:Fe;Fe+2Ag+=Fe2++2Ag;
(4)固体B为Ag,溶液B为硫酸亚铁,可得到硫酸亚铁晶体,故答案为:银;硫酸亚铁晶体.
本题解析:
本题难度:一般
5、选择题 如图,在盛有溴水的三支试管中分别加入苯、四氯化碳和酒精,振荡后静置,出现下列现象,正确的结论是
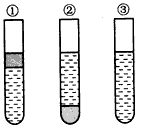
[? ]
A.①加入的是CCl4,②加苯,③加酒精
B.①加入的是酒精,②加CCl4,③加苯
C.①加入的是苯,②加CCl4,③加酒精
D.①加入的是苯,②加酒精,③加CCl4
参考答案:C
本题解析:
本题难度:简单