1、实验题 (11分)(1)为除去粗盐中的Ca2+、Mg2+、Fe3+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
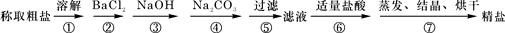
①第5步实验操作需要烧杯、____________、___________玻璃仪器。
②步骤2中,判断加入BaCl2已过量的方法是:?
??。
③除杂试剂BaCl2、NaOH、Na2CO3加入的顺序必须满足? ?。
④若先用盐酸调pH值再过滤,将对实验结果产生影响,其原因是_____________________________。
(2)为检验粗盐溶液中Cl-、SO42-请根据内容填空:
①首先检验?离子,应先加入过量的?。
②将所得混合物过滤,然后在溶液中加入试剂?检验另一离子。
参考答案:(11分)(1)①玻璃棒?漏斗?
②在2步骤后的上层清液中,再滴入BaCl2溶液,若溶液未变浑浊,则表明BaCl2已过量(其它合理答案也可)?(2分)?③Na2CO3在BaCl2后?(2分)④使部分沉淀溶解(2分)
(2)①SO42-,? Ba(NO3)(HNO3)?② AgNO3(HNO3)
本题解析:(1)①过滤需要烧杯、玻璃棒和漏斗。
②判断加入BaCl2已过量的方法是继续加入氯化钡,即在2步骤后的上层清液中,再滴入BaCl2溶液,若溶液未变浑浊,则表明BaCl2已过量。
③由于过量的氯化钡必需通过碳酸钠来除去,所以顺序必需是Na2CO3在BaCl2后面。
④由于盐酸钠溶解沉淀碳酸钡、碳酸钙和氢氧化镁,所以又引入杂质。
(2)①由于硫酸银也是难溶性的白色沉淀,所以首先检验SO42-,?所用试剂是硝酸酸化的硝酸钡。
②检验氯离子用硝酸酸化的硝酸银。
本题难度:一般
2、选择题 下列仪器中常用于物质分离的是
①漏斗;②量筒;③蒸馏烧瓶;④天平;⑤分液漏斗;⑥研钵;⑦蒸发皿
A.①③④
B.①②⑥
C.①③⑤⑦
D.①③⑥
参考答案:C
本题解析:物质的常用分离方法是过滤、蒸发、蒸馏和萃取等。过滤需要漏斗,蒸馏需要蒸馏烧瓶,萃取需要分液漏斗,蒸发需要蒸发皿,所以正确的答案选C。
本题难度:简单
3、实验题 下图是用自来水制取少量蒸馏水的简易装置,(加热及固定仪器略),其原理与教材中的实验完全相同。回答下列问题:

(1)左边大试管中要加入几片碎瓷片,其作用是?
(2)该装置中使用的玻璃管较长,其作用是?
(3)烧杯中还应该加入的物质是?
参考答案:(1)?防止爆沸?(2)?导气和冷凝?(3)?冰水
本题解析:在加热过程中,为防止受热液体剧烈跳动,需要加入碎瓷片来防止爆沸;玻璃管一方面起导气的作用,另一方面长导管能起冷凝作用;为使水蒸气液化,应该降低温度,所以应该加入冰水。
本题难度:一般
4、选择题 以下实验或操作不能达到目的的是
[? ]
A.用溴水鉴别苯乙醇、四氯化碳
B.准确称取0. 4000g的NaOH同体配成1000 mL浓度为0.01000mol/L的溶液
C.为除去苯中的少量苯酚,向混合物中加入适量的溴水后过滤
D.用激光笔检验淀粉溶液的丁达尔现象
参考答案:BC
本题解析:
本题难度:一般
5、选择题 能用分液漏斗进行分离的一组物质是
A.硝酸和水
B.乙醇和水
C.乙酸乙酯和水
D.乙酸和水
参考答案:C
本题解析:能用分液漏斗进行分离的溶液,一定是互不相容的。故答案选C
本题难度:简单