1、实验题 (4分)用酸式滴定管准确移取25.00mL某未知浓度的盐酸溶于一洁净的锥形瓶中,然后用0.20mol・L -1的氢氧化钠溶液(指示剂为酚酞).滴定结果如下:
?
| NaOH起始读数
| NaOH终点读数
|
第一次
| ? 0.10mL
| ? 18.60mL
|
第二次
| ? 0.30mL
| ? 18.00mL
|
(1)根据以上数据可以计算出盐酸的物质的量浓度为?mol・L-1.
(2)达到滴定终点的标志是?
参考答案:(4分)(1)0.1448 mol/L?(2)无色变粉红色且30s不变色
本题解析:(1)根据表中数据可知,两次消耗的氢氧化钠溶液体积分别是18.50ml和17.70ml,其平均值是18.10ml,所以盐酸的物质的量浓度是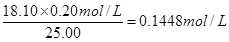 。
。
(2)由于酸不能使酚酞试液变色,而碱能使酚酞试液变红色,所以达到滴定终点的标志是无色变粉红色且30s不变色。
点评:由于一次实验误差太大,所以在进行中和滴定的有关计算时,应该要重复实验2~3次,然后取平均值即可。
本题难度:简单
2、选择题 25℃时,在等体积的① pH=0的H2SO4溶液,②0.05 mol?L?1的Ba(OH)2溶液,③pH=10的Na2S溶液,④pH=5的NH4NO3溶液中,发生电离的水的物质的量之比是( )
A.1:10:10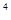 :10
:10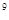
B.1:5:5×10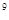 :5×10
:5×10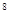
C.1:20:10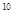 :10
:10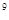
D.1:10:10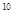 :10
:10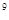
参考答案:D
本题解析:酸或碱都是抑制水的电离平衡的,且溶液中氢离子浓度或OH-浓度越大,对水的抑制程度越大。盐类水解是促进水的电离,所以发生电离的水的物质的量浓度(mol/L)分别是10-14、10-13、10-4、10-5,则发生电离的水的物质的量之比是1:10:10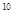 :10
:10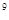 ,答案选D。
,答案选D。
点评:该题是中等难度的试题,侧重对学生能力的培养。该题的关键是明确酸、碱以及盐是如何影响水的电离平衡的,如何在结合水的电离平衡灵活运用即可,有利于培养学生的逻辑推理能力和应试能力,提升学生的学科素养
本题难度:简单
3、选择题 下列说法或表示法正确的是?
[? ]
A.由“C(石)→C(金);△H= +1.9 kJ/mol ”可知金刚石比石墨稳定
B.在101KPa时,1mol碳燃烧所放出的热量为碳的燃烧热
C.在101kPa时,2gH2完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g) = 2H2O(l);△H= -571.6kJ/mol
D.HCl和NaOH反应的中和热△H= -57.3kJ/mol,则H2SO4和Ca(OH)2反应的中和热为△H= -(2×57.3)kJ/mol
参考答案:C
本题解析:
本题难度:简单
4、选择题 下列说法正确的是(?)
A.pH=2和pH=1的硝酸中c(H+)之比为1:10
B.0.2 mol/L与0.1 mol/L醋酸中c(H+)之比为2:1
C.室温时,0.1mol/L 某一元酸HA在水中有0.1%发生电离,则该溶液的pH=4
D.25 ℃时,pH=13的1.0 L Ba(OH)2溶液中含有的OH- 数目为0.2NA
参考答案:AC
本题解析:硝酸为强酸,所以pH=2和pH=1的硝酸中c(H+)之比为1:10,故A正确,醋酸为弱酸,所以0.2 mol/L与0.1 mol/L醋酸中c(H+)之比不为2:1,故B错误;室温时,0.1mol/L 某一元酸HA在水中有0.1%发生电离,即c(H+)=0.1×0.1%=0.0001,所以pH=-lgc(H+)=4,故C正确;pH=13的1.0 L Ba(OH)2溶液中含有的OH- 数目为0.1NA ,故D错误,所以本题的答案选择AC。
点评:本题考查了强弱酸、碱的基础知识,属于对基础知识的考查,本题难度不大。
本题难度:简单
5、选择题 下列关于煤、石油、天然气等资源的说法正确的是(?)
A.煤的干馏是物理变化
B.石油分馏得到的汽油是纯净物
C.天然气是一种清洁的化石燃料
D.石油裂解的主要目的是为了得到更多的汽油
参考答案:C
本题解析:煤的干馏是化学变化,A不正确;石油分馏得到的汽油是混合物,B不正确;石油裂化的目的是为了提高轻质液体燃料的产量和质量,特别是提高汽油的产量,D不正确,裂解主要是为了得到各种化工原料,答案选C。
点评:该题是基础性试题的考查,试题侧重对基础知识的考查。该类试题常把化学知识与实际生产、生活、环境保护及科技前沿等问题结合起来,突出化学与可持续发展、环境保护的密切联系,综合考查学生分析问题、解决问题的能力。
本题难度:简单