1、选择题 氰(CN)2、硫氰(SCN)2、氧氰(OCN)2的化学性质相似,在化学上称为拟卤素。CN-、SCN-、OCN-的性质与卤素离子相似。已知:不同卤素原子能组成卤素互化物,如IBr;HSCN为强酸,HClO、HCN为弱酸。试回答下列各题。
(1)下列物质的电子式错误的是
[? ]
A.IBr 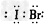
B.HClO 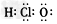
C.CN-
D.MgO 
(2)已知(OCN)2的电子式为: ,则下列SCN-的电子式正确的是
,则下列SCN-的电子式正确的是
[? ]
A.
B.
C.
D.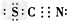
参考答案:(1)B
(2)C
本题解析:
本题难度:简单
2、选择题 根据下表提供的信息判断有关晶体的说法正确的是

[? ]
A.I和II均属分子晶体
B.I和IV融化时克服的粒子间的作用力相同
C.III中存在共价键、金属键和范德华力
D.II和IV都一定难溶于CCl4
参考答案:C
本题解析:
本题难度:简单
3、选择题 下列指定微粒的个数比为2:1的是?
[? ]
A. Be2+离子中的质子和电子
B. 21H原子中的中子和质子
C. NaOH晶体中的阳离子和阴离子
D. Na2O2固体中的阴离子和阳离子
参考答案:A
本题解析:
本题难度:简单
4、选择题 下列各组物质中,不互为同素异形体的是
A.金刚石和C60
B.红磷和P4
C.O2和O3
D.1H和2H
参考答案:D
本题解析:略
本题难度:一般
5、选择题 下列叙述正确的是( )
A.离子化合物可能含共价键,共价化合物中不含离子键
B.构成单质分子的微粒一定含有共价键
C.由非金属元素组成的化合物不一定是共价化合物
D.只有在活泼金属元素和活泼非金属元素化合时,才能形成离子键
参考答案:AC
本题解析:
本题难度:简单