1、选择题 ClO2是一种消毒杀菌效率高、二次污染小的水处理剂。实验室可通过以下反应制得ClO2:
2KClO3+H2C2O4+H2SO4 2ClO2↑+K2SO4+2CO2↑+2H2O下列说法正确的是
2ClO2↑+K2SO4+2CO2↑+2H2O下列说法正确的是
[? ]
A.KClO3在反应中失去电子
B.ClO2是氧化产物
C.H2C2O4在反应中被氧化
D.1 molKClO3参加反应有2mol电子转移
参考答案:C
本题解析:
本题难度:简单
2、选择题 氰酸HCNO可消除汽车尾气中的二氧化氮,有关反应的化学方程式为:8HCNO+6NO2=7N2+8CO2+4H2O,下列叙述中正确的是
A.氮气是还原产物,二氧化碳是氧化产物
B.HCNO中碳元素被氧化
C.1molHCNO参加反应失去3mol电子
D.氧化产物与还原产物物质量比为1:1
参考答案:C
本题解析:选项A不正确,氮气既是氧化产物,也是还原产物;碳元素的化合价不变,因此CO2不是氧化产物,选项B不正确;反应物HCNO中氮元素的化合价从-3价升高到0价,失去3个电子,所有选项C正确;NO2中氮元素的化合价从+4价降低到0价,得到4个电子,因此氧化产物与还原产物物质量比为4:3,选项D不正确,答案选C。
本题难度:一般
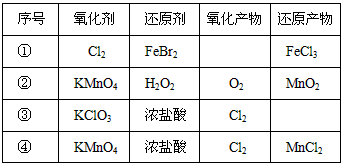
3、选择题 根据下表信息,下列叙述中正确的是
[? ]
A.表中①反应的氧化产物只能有FeCl3
B.表中②生成1mol的O2将有4mol的电子转移
C.表中④的离子方程式配平后,H+的化学计量数为16
D.表中③还原产物是KCl
参考答案:C
本题解析:解析:
A.表中①Fe3+Br_都有可能被氯气所氧化,氧化产物可能有Br2也可能有FeCl3?,故错;
B.表中②生成1mol的O2全由过氧化氢被氧化所得,将有2mol的电子转移,故错
C.表中④的离子方程式配平后为2MnO4-+16H++14Cl-=7Cl2+2Mn2++3H2O,H+的化学计量数为16,故正确;
D.表中③氧化产物和还原产物都是Cl2,故错。
故选:C
本题难度:简单
4、填空题 (6分)某一反应体系中的物质有:HCl、SnCl2、H2SnCl6、As、H3AsO3、H2O,
已知:As是产物之一。
(1)写出并配平该反应的化学方程式 ______________?
(2)在反应中,每转移1 mol电子,消耗(或生成)HCl_______mol;
(3)下列叙述正确的是_____________(填写序号)。
a.在相同条件下,第VIIA族元素的阴离子的还原性从上到下逐渐增强
b.Sn和Pb位于同一主族,其+4价的化合物均很稳定
c.在相同条件下,还原性顺序:S2->I->Fe2+>Br->Cl-
d.在上述反应中,氧化性:SnCl2?>As,还原性:H3AsO3>H2SnCl6
参考答案:(1)12HCl+3SnCl2+2H3AsO3="2As+6H2O+3H2SnCl6?" (2分)(2)2 (2分)(3 )ac? (2分)
)ac? (2分)
本题解析:略
本题难度:一般
5、选择题 下列说法正确的是(? )
A.置换反应都是氧化还原反应
B.复分解反应可能是氧化还原反应
C.化合反应一定是氧化还原反应
D.分解反应都是氧化还原反应
参考答案:A
本题解析:置换反应有单质参加和生成,一定存在元素化合价的变化,故一定属于氧化还原反应。
本题难度:简单