|
高中化学知识点讲解《认识晶体》考点强化练习(2019年押题版)(八)
2020-07-08 00:30:05
【 大 中 小】
|
1、填空题 (8分)
 ?铜合金是人类使用最早的金属材料,铜在化合物中常见的化合价有+1、+2价,能形成多种铜的化合物。 ?铜合金是人类使用最早的金属材料,铜在化合物中常见的化合价有+1、+2价,能形成多种铜的化合物。
(1)基态铜离子(Cu+)的电子排布式为?。
(2)+2价铜可形成化合物[Cu(NH3)4]SO4,下列各项中,该物质
中不含的化学键类型是?(填字母序号)。
A.离子键
B.金属键
C.配位键
D.共价键
| (3)+1价铜形成的配合物溶液能吸收CO和乙烯(CH2=CH2),
乙烯分子中六个原子在同一平面内,则乙烯分子中C原子
的杂化轨道类型为?。
(4)金属铜的晶体类型属于金属晶体,其晶胞结构如右图所示,该晶胞实际拥有?个铜原子。
参考答案: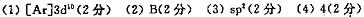
本题解析:略
本题难度:一般
2、选择题 下列各晶体中,含有的化学键的类型相同且晶体类型也相同的一组是
A.SiO2和SO2
B.SiO2和 NaCl
C.NaCl和 HCl
D.CCl4和CH4
参考答案:D
本题解析:略
本题难度:简单
3、填空题 某离子晶体晶胞结构如下图所示,x位于立方体的顶点,Y位于立方体中心。试分析
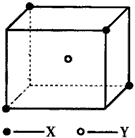
(1)晶体中每个Y同时吸引着__________个X,每个x同时吸引着______个Y,该晶体的化学式为__________ 。
(2)晶体中在每个X周围与它最接近且距离相等的X共有__________个。
(3)晶体中距离最近的2个X与1个Y形成的夹角∠XYX的度数为__________。
(4)设该晶体的摩尔质量为M g・mol-1,晶体密度为ρ・cm-3,阿伏加德罗常数为NA则晶体中两个距离最近的X中心间的距离为__________。
参考答案:(1)4;8;XY2(或Y2X)
(2)12
(3)109°28"
(4)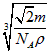
本题解析:
本题难度:一般
4、填空题 决定物质性质的重要因素是物质结构。请回答下列问题。
(1)已知A和B为第三周期元素,其原子的第一至第四电离能如下表所示
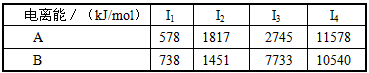
A的化合价____(填“>”“<”或“=”)B的化合价。
(2)实验证明:KCl、MgO、CaO、TiN这4种晶体的结构与NaCl晶体结构相似(如左下图所示),其中3种离子晶体的晶格能数据如下表:
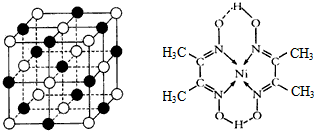
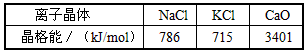
则该4种离子晶体(不包括NaCl)熔点从高到低的顺序是:________。 其中MgO晶体中一个Mg2+周围和它最邻近且等距离的Mg2+有____个。
(3)金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好。离子型氧化物V2O5和CrO2中,适合作录音带磁粉原料的是____________。
(4)某配合物的分子结构如上图(右)所示,则N原子的杂化方式为__________;基态Ni原子的电子排布式___________。
参考答案:(1)>
(2)TiN>MgO>CaO>KCl;12
(3)CrO2
(4)sp2;[Ar]3d84s2
本题解析:
本题难度:一般
5、选择题 铁有δ、γ、α三种同素异形体,如下图所示,三种晶体在不同温度下能发生转化。下列说法不正确的是( )

A.将铁加热到1500°C分别急速冷却和缓慢冷却,得到的晶体类型相同
B.α-Fe晶体中与每个铁原子等距离且最近的铁原子有6个
C.若δ-Fe晶胞边长为a cm,α-Fe晶胞边长为b cm,则两种晶体密度比为2b3:a3
D.δ-Fe晶体中与每个铁原子等距离且最近的铁原子有8个
参考答案:A
本题解析:根据已知信息可知,将铁加热到1500°C分别急速冷却和缓慢冷却,得到的晶体分别是α-铁和δ-铁,类型不相同,选项A不正确。根据晶胞的结构特点可知,选项B正确;δ-Fe晶胞中含有2个铁原子,α-Fe晶胞中含有1个碳原子,所以两种晶体密度比为2b3:a3,选项C正确;题意根据晶胞可知,选项D正确,答案选A。
点评:该题是高考中的常见题型和考点,属于中等难度试题的考查,试题综合性强,侧重对学生能力的培养和训练,有利于培养学生的逻辑推理能力、自学能力和知识的迁移能力,提高学生灵活运用基础知识解决实际问题的能力。
本题难度:简单
|