1、选择题 借助于化学方法,分子是可以再分的,而原子不能用化学方法再分为更小的微粒。下列实验事实最能体现上述论点的是
A.食盐固体溶于水消失
B.盛浓盐酸的试剂瓶打开冒白雾
C.干冰露置在空气中逐渐消失
D.红色氧化汞粉末受热分解成氧气和汞
参考答案:D
本题解析:试题分析:此题主要考查物质的化学变化。答题时,需充分理解题意。题干中给出的信息“分
子是可以再分的,而原子不能用化学方法再分为更小的微粒”实际上就说出了化学变化的实质。所以,对四个选项的分析,首先应从“物理变化”、“化学变化”入手。
对于A选项,食盐溶于水,应属于物理变化;
对于B选项,浓盐酸冒白烟,主要体现的是浓盐酸的挥发性,挥发性属于物理性质,因此,B选项所描述的也是一种物理变化;
对于C选项,干冰在空气中逐渐消失,是干冰的升华现象,也属于物理变化;
对于D选项,氧化汞受热分解,则是一种化学变化。在这一过程中,氧化汞受热分解为汞原子和氧原子,而这两种原子不可再分为更小的粒子,重新结合形成新的物质,即氧气和汞单质。
考点:化学变化的实质;物理变化;化学变化
点评:1、本题主要考查化学变化的实质:“在化学变化中,分子断裂成为原子,原子重新
组合,形成新的分子。”
2、区别物理变化与化学变化的根本在于是否有新物质生成,有新物质生成的变化则为化学变化,否则为物理变化。另外,区分化学变化与物理变化也可以从描述所体现的性质入手,体现物理性质的则为物理变化;体现化学性质的则为化学变化。
本题难度:困难
2、选择题 查阅资料发现,金属钠不仅能够跟氧气和水反应,还能跟很多种其他物质发生反应,其中包括与酒精在常温下反应,要研究金属钠和酒精反应的性质以及它与金属钠跟水反应的异同点,下列的研究方法中用不着的是
A.分类法
B.观察法
C.实验法
D.比较法
参考答案:A
本题解析:试题分析:要研究金属钠和酒精反应的性质以及它与金属钠跟水反应的异同点,可以通过观察法、实验法或比较法完成,而与分类法是无关系的,答案选A。
考点:考查化学研究的一般方法
点评:本题属于基础性试题,主要是考查学生对化学研究方法的理解,有利于调动学生的选项积极性和学习兴趣。
本题难度:一般
3、选择题 相同质量的下列物质,放入相同体积的过量水中,所得溶液的溶质质量分数最大的是
A.Na
B.Na2O
C.NaOH
D.Na2O2
参考答案:A
本题解析:试题分析:设四种物质的质量分别为m,水的质量分别为n
A中
2Na + 2H2O = 2NaOH+H2↑
46?80?2
m?X1?Y1
即X1= 、Y1=
、Y1=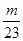
所以所得溶液的溶质质量分数为 
B中?Na2O + H2O = 2NaOH
62?80
m?X2
即X2=
所以所得溶液的溶质质量分数为 
C中所得溶液的溶质质量分数为 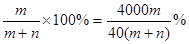 m
m
D中?2Na2O2+2H2O=4NaOH+O2↑
156?160?32
m?X3?Y3
即X3=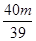 、Y3=
、Y3=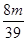
所以所得溶液的溶质质量分数为
通过计算可知四种溶液的溶质质量分数的分子的质量相等,而分母的质量为(22m+23n)<31(m+n)<(31m+39n)<40(m+n),所以A所得溶液的溶质质量分数最大,答案选A。
考点:考查质量分数的有关计算
点评:该题难度较大,主要是计算量大,不易得分。本题主要是通过化学方程式的有关计算,训练学生的计算能力,以及分析问题解决实际问题的能力。
本题难度:一般
4、选择题 同温同压下,等质量的SO2气体和SO3气体相比较,下列叙述中正确的是
A.密度比为4:5
B.物质的量之比为4:5
C.体积比为1:1
D.原子数之比为3:4
参考答案:A
本题解析:分析:根据质量计算气体的物质的量,可得物质的量之比,根据分子组成可得原子数之比,同温同压下,气体的物质的量之比等于体积之比,密度之比等于相对分子质量之比.
解答:A、由n=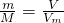 可知,
可知, ,在相同条件下气体的相对分子质量之比等于密度之比,
,在相同条件下气体的相对分子质量之比等于密度之比,
所以两种气体的密度之比为:64:80=4:5,故A正确;
B、设气体的质量为m,则n(SO2)= mol,n(SO3)=
mol,n(SO3)=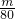 mol,所以物质的量之比为=
mol,所以物质的量之比为= :
: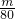 =80:64=5:4,故B错误;
=80:64=5:4,故B错误;
C、根据V=n?Vm可知,同温同压下,气体的物质的量之比等于体积之比,所以两种气体体积之比等于5:4,故C错误;
D、根据分子组成可知,两种气体的原子数之比为:5×3:4×4=15:16,故D错误.
故选A.
点评:本题考查阿伏加德罗定律及推论,题目难度中等,注意物质的量与体积、密度、原子数目的计算公式的运用.
本题难度:困难
5、选择题 NA表示阿伏加德罗常数的值,下列说法中正确的是
A.100mL?lmol?L-1Na2CO3溶液中溶质离子的总数为0.3NA
B.若120g的墨粉(只含碳)能打a个字,则平均每个字约含有个碳原子
C.25℃、l01?kPa时,0.1NA个H2分子完全燃烧生成液态水,放出akJ热量,表示氢气燃烧热的热化学方程式为△H=+1OakJ?mol-1
D.常温下28g14CO中含有14NA个电子
参考答案:B
本题解析:分析:A、碳酸根离子水解;
B、120g的墨粉(只含碳)能打a个字,一个字需要墨粉的质量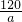 ,碳原子数=
,碳原子数= =
=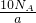 ;
;
C、氢气燃烧热是放热反应,焓变为负值;
D、质量换算物质的量,结合质子数+中子数=质量数计算电子数.
解答:A、100mL?lmol?L-1Na2CO3溶液中溶质离子的总数小于0.3NA,故A错误;
B、120g的墨粉(只含碳)能打a个字,一个字需要墨粉的质量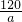 ,碳原子数=
,碳原子数= =
=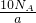 ;则平均每个字约含有
;则平均每个字约含有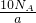 个碳原子,故B正确;
个碳原子,故B正确;
C、表示氢气燃烧热的热化学方程式为H2(g)+ O2(g)=H2O(l)△H=-1OakJ?mol-1 ,故C错误;
O2(g)=H2O(l)△H=-1OakJ?mol-1 ,故C错误;
D、常温下28g14CO物质的量为 ,小于1mol,含有的电子数小于14NA,故D错误;
,小于1mol,含有的电子数小于14NA,故D错误;
故选B.
点评:本题考查阿伏伽德罗常的应用,主要是盐类水解应用,质量换算物质的量计算微粒数,热化学方程式判断,题目难度中等.
本题难度:简单