1、选择题 下列反应属于取代反应的是(?)
A.乙醇和浓H2SO4加热至140 ℃
B.乙醇和氢溴酸的反应
C.乙醇的催化氧化
D.由乙醇制乙烯
参考答案:AB
本题解析:A项,2CH3CH2OH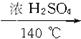 CH3CH2―O―CH2CH3+H2O;B项,CH3CH2OH+HBr
CH3CH2―O―CH2CH3+H2O;B项,CH3CH2OH+HBr  CH3CH2Br+H2O;C项,2CH3CH2OH+O2
CH3CH2Br+H2O;C项,2CH3CH2OH+O2 2CH3CHO+2H2O;D项,CH3CH2OH
2CH3CHO+2H2O;D项,CH3CH2OH  CH2==CH2+H2O。
CH2==CH2+H2O。
本题难度:简单
2、填空题 某有机物A?的分子式为C4H10O,且1molA能与足量金属钠反应生成0.5mol?H2(标准状况),
(1)试写出A可能的结构简式.
(2)任选一种结构写出在铜作催化剂加热条件下的氧化反应方程式.
参考答案:分子式为C4H10O,且1molA能与足量金属钠反应生成0.5mol?H2的是丁醇,存在同分异构体,有4种,即:
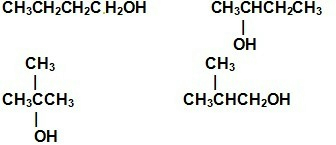
,故答案为:

;
(2)能在铜作催化剂加热条件下发生氧化反应的醇只能是伯醇,符合要求的是:CH3CH2CH2CH2OH和

,反应的方程式为:
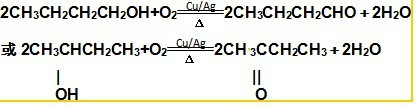
,故答案为:

.
本题解析:
本题难度:一般
3、填空题 正丁醚常用作有机反应的溶剂。实验室制备正丁醚的主要实验装置如下图:
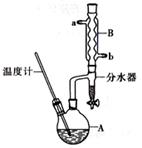
反应物和产物的相关数据如下
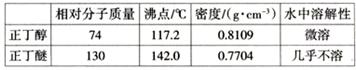
合成正丁醚的步骤:
①将6 mL浓硫酸和37 g正丁醇,按一定顺序添加到A中,并加几粒沸石。
②加热A中反应液,迅速升温至135℃,维持反应一段时间。分离提纯:
③待A中液体冷却后将其缓慢倒入盛有70 mL水的分液漏斗中,振摇后静置,分液得粗产物。
④粗产物依次用40 mL水、20 mL NaOH溶液和40 mL水洗涤,分液后加入约3 g无水氯化钙颗粒,静置一段时间后弃去氯化钙。
⑤将上述处理过的粗产物进行蒸馏,收集馏分,得纯净正丁醚11 g。?
请回答:
(1)步骤①中浓硫酸和正丁醇的添加顺序为______________________________。
写出步骤②中制备正丁醚的化学方程式______________________________。
(2)加热A前,需先从__________(填“a”或“b”)口向B中通入水。
(3)步骤③的目的是初步洗去?,振摇后静置,粗产物应从分液漏斗的?(填“上”或“下”)口分离出。
(4)步骤④中最后一次水洗的目的为______________________________。
(5)步骤⑤中,加热蒸馏时应收集__________(填选项字母)左右的馏分。
a.100℃? b. 117℃? c. 135℃? d.142℃
(6)反应过程中会观察到分水器中收集到液体物质,且分为上下两层,随着反应的进行,分水器中液体逐渐增多至充满时,上层液体会从左侧支管自动流回A。分水器中上层液体的主要成分为__________,下层液体的主要成分为__________。(填物质名称)
(7)本实验中,正丁醚的产率为__________。
参考答案:(1)先加正丁醇,再加浓H2SO4或将浓H2SO4滴加到正丁醇中
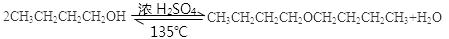
(2)b
(3)浓H2SO4?上
(4)洗去有机层中残留的NaOH及中和反应生成的盐NaSO4
(5)d
(6)正丁醇?水
(7)33.85%
本题解析:(1)步骤①中浓硫酸和正丁醇的添加顺序为先加正丁醇,再加浓H2SO4。步骤②中制备正丁醚是利用正丁醇的分子间脱水反应得到,方程式为 ;(2)冷凝管应从下口进水,故需先从b口向B中通入水;(3)步骤③水洗的目的是初步洗去浓H2SO4,振摇后静置,粗产物应从分液漏斗的上口分离出;(4)步骤④中最后一次水洗的目的为洗去有机层中残留的NaOH及中和反应生成的盐NaSO4;(5)因为正丁醚的沸点为142℃,故步骤⑤中,加热蒸馏时应收集142℃左右的馏分,选d;(6)正丁醇易挥发,且不溶于水,密度小于水,故上层应为正丁醇,下层为水;(7)按照方程式37 g正丁醇可得到正丁醚32.5g,故正丁醚的产率为11g/32.5g = 33.85%。
;(2)冷凝管应从下口进水,故需先从b口向B中通入水;(3)步骤③水洗的目的是初步洗去浓H2SO4,振摇后静置,粗产物应从分液漏斗的上口分离出;(4)步骤④中最后一次水洗的目的为洗去有机层中残留的NaOH及中和反应生成的盐NaSO4;(5)因为正丁醚的沸点为142℃,故步骤⑤中,加热蒸馏时应收集142℃左右的馏分,选d;(6)正丁醇易挥发,且不溶于水,密度小于水,故上层应为正丁醇,下层为水;(7)按照方程式37 g正丁醇可得到正丁醚32.5g,故正丁醚的产率为11g/32.5g = 33.85%。
本题难度:一般
4、选择题 有机化学知识在生活中应用广泛,下列说法不正确的是( )
A.利用天然气做燃料可以有效地减少“温室效应”的气体产生
B.由于乙醇能够溶解很多有机物和无机物,所以可用乙醇提取中药的有效成分
C.用灼烧的方法可以鉴别毛织物和棉织物
D.油脂是产生能量最高的营养物质,在饮食中不必控制油脂的摄入量
参考答案:D
本题解析:
本题难度:简单
5、选择题 2001年9月1日将执行国家食品卫生标准规定,酱油中3氯丙醇(ClCH2CH2CH2OH)含量不得超过1 ppm。相对分子质量为94.5的氯丙醇(不含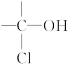 结构)共有(?)
结构)共有(?)
A.2种
B.3种
C.4种
D.5种
参考答案:B
本题解析:相对分子质量为94.5的氯丙醇的分子式为C3H7OCl,其可能的结构简式为:
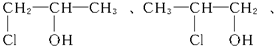
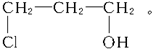
本题难度:简单