1、选择题 下列物质既能发生消去反应,又能氧化成醛的是
[? ]
A. 
B. 
C. 
D. 
参考答案:C
本题解析:
本题难度:简单
2、选择题 完全燃烧一定质量的无水乙醇,放出的热量为Q,已知为了完全吸收生成的二氧化碳,消耗掉8mol・L-1的氢氧化钠溶液50mL,则相同条件下1 mol无水乙醇燃烧放出的热量不可能是[ ]
A.小于5Q
B.5Q
C.5Q~10Q
D.10Q
参考答案:A
本题解析:利用生成的CO2消耗掉8mol・L-1的氢氧化钠溶液50mL,可计算出二氧化碳的物质的量,即得出二氧化碳的物质的量与放出的热量的关系,再利用完全燃烧1摩尔无水乙醇生成2摩尔二氧化碳来分析放出的热量.因生成的CO2消耗掉8mol・L-1的氢氧化钠溶液50mL ,氢氧化钠的物质的量为0.4 mol,则最多吸收的二氧化碳为0.4 mol根据质量守恒完全燃烧的无水乙醇最多为0.2 mol则相同条件下1 mol无水乙醇燃烧放出的热量大于等于5Q不可能小于5Q,故选A
本题难度:一般
3、选择题 相同的反应物若使用不同的反应溶剂,可得到不同的产物。如:
C2H5OH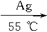 CH3CHO+H2↑
CH3CHO+H2↑
2C2H5OH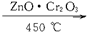 CH2==CH―CH==CH2+H2↑+2H2O
CH2==CH―CH==CH2+H2↑+2H2O
2C2H5OH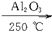 C2H5OC2H5+H2O
C2H5OC2H5+H2O
又知C2H5OH在活性铜催化下,可生成CH3COOC2H5及其他产物,则其他产物可能为(?)
A.H2
B.CO2
C.H2O
D.H2和H2O
参考答案:A
本题解析:根据质量守恒定律可写出:2C2H5OH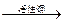 CH3COOC2H5+2H2↑。
CH3COOC2H5+2H2↑。
本题难度:简单
4、选择题 二甘醇可用作溶剂、纺织助剂等,一旦进入人体会导致急性肾衰竭,危及生命。二甘醇的结构简式是
HO-CH2CH2-O-CH2CH2-OH。下列有关二甘醇的叙述正确的是
[? ]
A.不能发生消去反应
B.能发生取代反应
C.能溶于水,不溶于乙醇
D.符合通式CnH2nO3
参考答案:B
本题解析:
本题难度:一般
5、填空题 (本题共8分)酒后驾车已成为一个社会问题。检测驾驶人员呼气中酒精浓度(BrAC)的方法有多种。
1.早期是利用检测试剂颜色变化定性判断BrAC,曾用如下反应检测BrAC:
3CH3CH2OH+2KMnO4→3CH3CHO+2MnO2+2KOH+2H2O 。
上述反应中发生还原反应的过程是__________ →___________。?
2.已知KMnO4在酸性条件下氧化性增强,能得到更多的电子,若在稀硫酸中反应的氧化产物为乙酸,则还原产物为___________;若反应产生了12.0 mg乙酸,则转移的电子数目是________。
3.受上述方法启发,后来用五氧化二碘的淀粉溶液检测BrAC,乙醇被氧化为乙醛,该反应的化学方程式为__________________________________________________。
4.1994年美国首次批准使用唾液酒精含量检测方法,成为血液、呼气之后的第三种检测手段。其原理是在乙醇氧化酶作用下,乙醇与氧气反应生成乙醛和过氧化氢,判断该条件下乙醇、氧气、乙醛和过氧化氢四种物质中氧化性最强的物质是________(填写化学式)。
参考答案:(本题共8分,每小题2分)
1.KMnO4?MnO2。
2. MnSO4; 4.816?1020或0.0008NA(2分)。?
3.I2O5+5CH3CH2OH?I2+5CH3CHO+5H2O(2分)
4.O2
本题解析:2.C2H6O→C2H4O2,可通过碳的化合价求电子的转移。根据H为+1、O为+2价,可求得碳的化合价从-2价升到0价。12.0 mg乙酸为0.0002mol,则转移的电子为:0.0002×2×2mol=0.0008mol
本题难度:简单