1、选择题 酸式盐NaHY的水溶液中,HY-的电离程度小于HY-的水解程度。下列有关叙述正确的是? ( )
A.HY-水解方程式为:HY-+ H2O H3O++ Y2-
H3O++ Y2-
B.在该盐的溶液中离子浓度大小关系为:c(Na+) >c(Y2-) >c(HY-) >c(OH-) >c(H+)
C.H2Y的电离方程式为:H2Y+H2O HY-+H3O+
HY-+H3O+
D.在该盐的溶液中:c(Na+) >c(HY-) >c(Y2-)>c(OH-)>c(H+)
2、选择题 下列解释实验事实的方程式不正确的是
A.0.1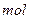 /L
/L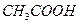 溶液的PH>1:
溶液的PH>1: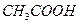
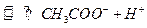
B.“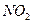 球”浸泡在冷水中,颜色变浅2
球”浸泡在冷水中,颜色变浅2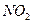 (g)
(g)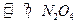 (g)△H<0
(g)△H<0
(红棕色)(无色)
C.铁溶于稀硝酸,溶液变黄:3Fe+8H++2N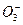
 3Fe2++2NO↑+4H2O
3Fe2++2NO↑+4H2O
D.向Na2CO3溶液中滴入酚酞溶液,溶液变红: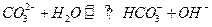
3、选择题 下列过程或现象与盐类的水解无关的是
A.加热氯化铁溶液的颜色变深
B.CaCO3的饱和溶液pH约为9.3
C.0.1 mol/L AlCl3溶液中c(Al3+)<0.1 mol/L
D.NaHCO3做发酵粉时加入柠檬酸后效果更好
4、填空题 Na2SO3和NaClO两种钠盐分别溶于水后,溶液的pH均大于7,露置于空气中相当一段时间后(不考虑水分挥发)溶液pH都近似为7。这两种溶液呈碱性的原因分别是:_______________________、________________________(用离子方程式表示)。久置呈中性的原因是_____________________________________________________________________。
5、选择题 缓冲溶液可以抗御少量酸碱对溶液pH的影响,Na2HPO4/Na3PO4的混合溶液可以将体系的pH稳定在11.3~13.3之间,是一种常用的缓冲溶液。下列有关该缓冲溶液的说法错误的是
A.加入少量强碱,发生反应HPO42―+OH―
B.加入少量强酸,发生反应HPO43―+H+
C.c(Na+)+c(H+)=c(OH―)+c(H?2PO4―)+2c(HPO42―)+3c(PO43-)
D.c(Na+)/2>c(PO43―)+c(HPO42―)+c(H2PO4―)+c(H3PO4)>c(Na+)/3